来源:好本子
细胞衰老一直都是肿瘤微环境中经久不衰的话题,目前已经成为科学研究的热门关注点之一,中标率也在逐年上升,已成为国自然的「香饽饽」。
浙江大学徐平龙/夏冰团队于 2024 年 2 月发表在 Science Advances 杂志上,题为 IRF3 activates RB to authorize cGAS-STING-induced senescence and mitigate liver fibrosis 的一篇文章。本研究利用两种小鼠肝纤维化模型,结合免疫学、遗传学及药理学方法,发现 cGAS-STING 信号在诱导细胞衰老中发挥重要作用,并揭示其在限制肝纤维化方面意想不到的生物学作用。
 图源:Science Advances
图源:Science Advances研究背景
细胞衰老是细胞生命历程的关键阶段之一,细胞的衰老死亡与新生细胞的生长之间的动态平衡是维持机体正常生命活动的基础。大量的研究报道已证明细胞衰老参与多种疾病的病理过程,研究并阐明细胞衰老的机制对治疗人类疾病具有重要意义。
cGAS-STING 信号的破坏或过度激活会导致感染性疾病、自身免疫性疾病和自身炎症性疾病以及癌症。cGAS-STING 驱动细胞衰老的发现是衰老研究的重大进展之一。然而,除已被报道的一种非规范的 cGAS-STING-PKR 样内质网激酶 (PERK) 途径在 mRNA 翻译水平上控制细胞衰老外,STING 诱导衰老的潜在机制尚不清楚。因此,本研究旨在探讨 cGAS-STING 信号在诱导细胞衰老的作用机制。
研究思路
在本研究中,研究人员首先基于文献研究 cGAS-STING 关键信号成分在衰老过程中的作用,接着发现 cGAS-STING-IRF3 和 p16INK4a-RB 通路在 DNA 损伤引发的衰老中起着至关重要的作用,通过这一结果建立起两信号通路在调节细胞衰老中的联系并阐明 IRF3 驱动细胞衰老背后的分子机制。最后通过四氯化碳 (CCl4) 和胆管结扎 (BDL) 诱导的小鼠肝纤维化模型表明全身性 IRF3 基因敲除或在肝星状细胞中条件性敲除 IRF3 都能够加剧肝脏的纤维化水平。 研究结果
1. IRF3 在启动细胞衰老中起关键作用
cGAS-STING 通路被认为是启动细胞衰老的关键触发因素,但其潜在机制尚不清楚。为探讨潜在机制,研究人员首先研究 cGAS-STING 关键信号成分 cGAS、STING、TANK 结合激酶 1(TBK1) 和 IRF3 在衰老过程中的作用。羟基脲 (HU) 是一种明确的 cGAS-STING 信号和细胞衰老的诱导剂,用羟基脲 (HU) 处理肠道上皮 DLD1 细胞,激活 STING 信号并导致 TBK1 和 IRF3 的磷酸化 (图 1A)。IRF3 在长时间观测期间保持持续活跃 (图 1A)。
IRF3 基因敲除显著抑制 DLD1 细胞中 DNA 损伤诱导的衰老,而重新引入 IRF3 可以逆转这一效应 (图 1B 和 C)。上述结果表明,cGAS-STING-IRF3 信号在诱导 DNA 损伤后的细胞衰老中起着显著作用。为进一步表征 IRF3 在 HU 诱导的衰老中的作用,研究人员进行 mRNA 测序转录组分析。HU 处理后观察到大量基因表达变化 (图 1D)。基因集富集分析显示,IRF3 KO 细胞中与细胞衰老标志物相关的基因显著减少 (图 1E)。
HU 处理后,WT 细胞中编码 SASP 因子如 CCL2、CXCL1 和 IL-8 的 mRNA 的表达明显增强,而 IRF3 KO DLD1 细胞中无明显变化 (图 1F)。考虑到细胞衰老的不同触发因素,研究人员还研究 IRF3 缺失在不同细胞背景下的影响,包括用于评估复制性衰老的 MRC-5 人胚胎成纤维细胞 (图 1 G) 以及用于评估氧应激诱导的衰老的 WT 和 IRF3 鼠的自发永生化原代 MEFs(图 1 H)。上述结果表明,IRF3 在各种上游刺激诱导的衰老过程中发挥着关键作用。
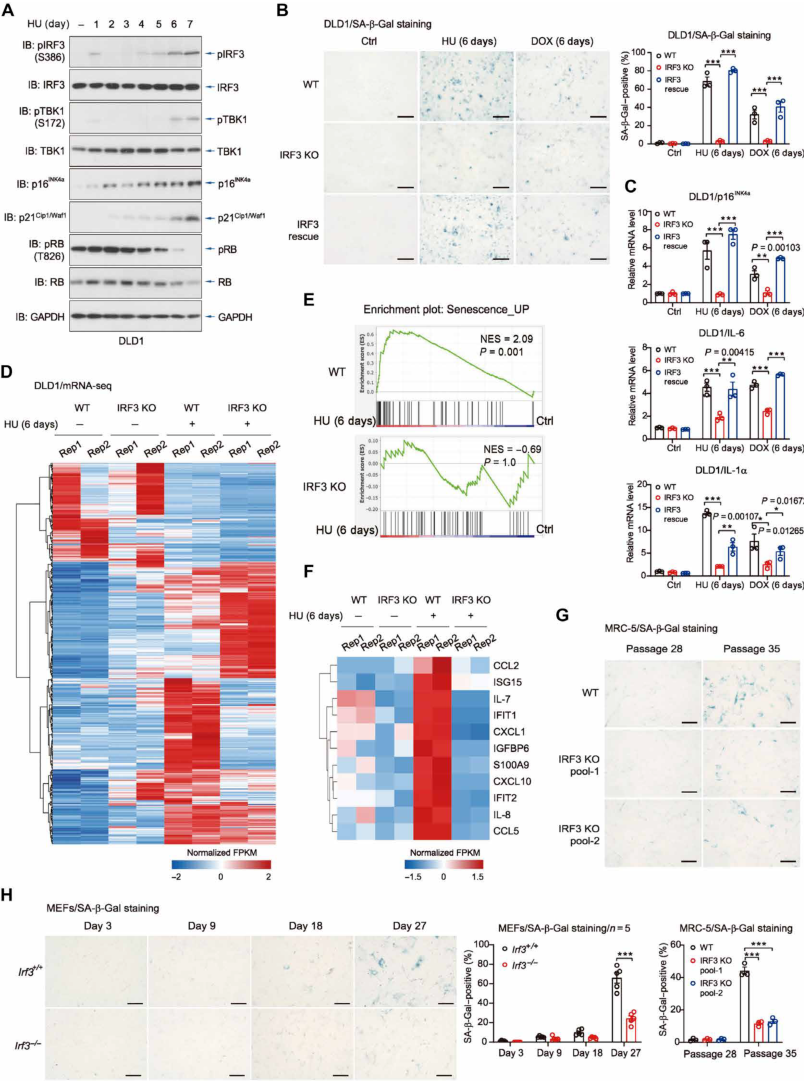 图 1 IRF3 缺失可减少细胞衰老表型
图 1 IRF3 缺失可减少细胞衰老表型2. IRF3 通过 p16INK4a-RB 途径调控细胞衰老
已知 IFN-α 可激活下游 Janus 激酶信号转导器和转录信号激活因子,但未能逆转 IRF3 KO 细胞的衰老损伤 (图 2A 和 B)。考虑到 IRF3 KO 还降低促衰老的 SASP 因子如 IL-6 和 IL-1α 的表达。研究人员用衰老细胞 (MS) 或重组 IL-6 培养基处理 IRF3 KO 细胞。这种处理在一定程度上模拟 IRF3 诱导的衰老,但它未能有效地恢复 IRF3 KO 细胞的衰老表型 (图 2C 和 D)。
上述观察结果表明,IRF3 在衰老诱导过程中除在细胞因子产生中的作用外,还具有重要的调节功能。CDK4/6 激酶是 p16INK4a-RB 通路中 RB 磷酸化的关键,其抑制可导致 RB 低磷酸化并引发衰老。值得注意的是,引入 palbociclib(CDK4/6 抑制剂) 显著逆转 IRF3 KO DLD1 细胞中受抑制的衰老表型 (图 2E 和 F)。此外,RB 的基因敲除几乎完全抑制 HU 诱导的衰老 (图 2 G 和 H)。这说明强调 p16INK4a-RB 通路在 DNA 损伤引发的衰老中起着至关重要的作用。这些发现建立起 cGAS-STING-IRF3 和 p16INK4a-RB 信号通路在调节细胞衰老中的联系。
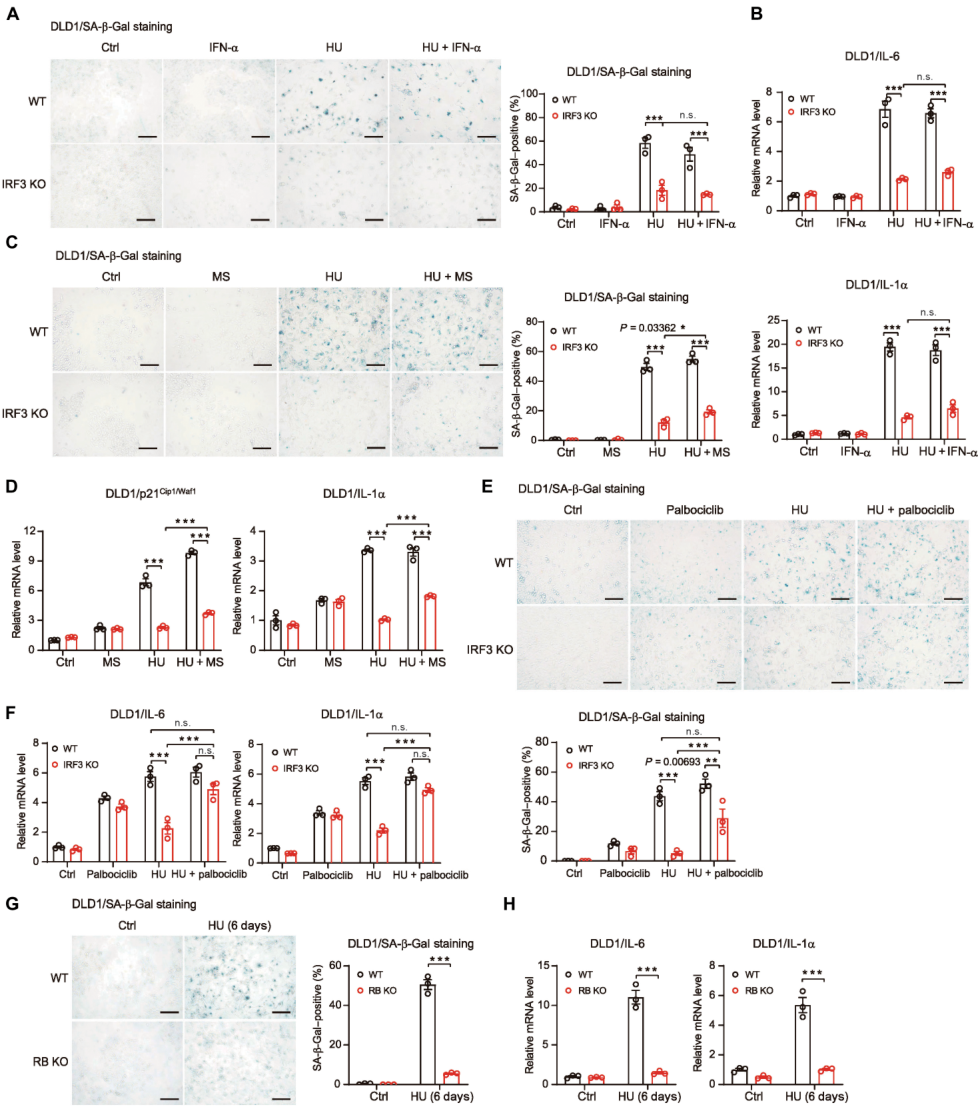 图 2 IRF3 通过 p16INK4a-RB 途径控制衰老
图 2 IRF3 通过 p16INK4a-RB 途径控制衰老3. IRF3 与细胞衰老的关键调控因子 RB 相关
为阐明 IRF3 驱动细胞衰老背后的分子机制,研究人员构建稳定表达 IRF3 的 DLD1,并使用质谱法鉴定潜在的 IRF3 相互作用蛋白。通过公共数据库数据发现衰老的中心调节因子 RB 是一个重要的 IRF3 标志物 (图 3A)。共免疫沉淀实验表明内源性 IRF3 和 RB 在 DNA 损伤诱导的衰老细胞中存在相互作用 (图 3B)。邻近结联实验 (PLA) 同样证实衰老细胞中内源性 IRF3 和 RB 蛋白存在关联 (图 3C)。
与 WT 相比,IRF3 的激活形式 (IRF35D) 与 RB 表现出强烈的相互作用 (图 3D)。此外,RB 还与 IRF7 相互作用 (图 3D)。为确定 RB 和 IRF3 之间相互作用的特定结构域,研究人员使用一系列 RB 和 IRF3 截断突变体进行结构域映射分析发现 IRF3 的干扰素激活结构域 (IAD) 和 RB 的口袋 B 结构域 (RB-B) 对它们的相互作用至关重要 (图 3E-G)。
通过检测 IRF3 突变体,研究人员发现 IRF3 S221A 突变 (图 3 H) 保留了诱导 IFN 基因的典型转录能力且丧失结合 RB 的能力 (图 3I)。相反,IRF3 R78A/R86A 突变影响 DNA 结合域并抑制 IFN 信号激活,但仍然保留结合 RB 的能力 (图 3 H-I)。这些发现表明,与 RB 的相互作用独立于 IRF3 的经典转录功能。
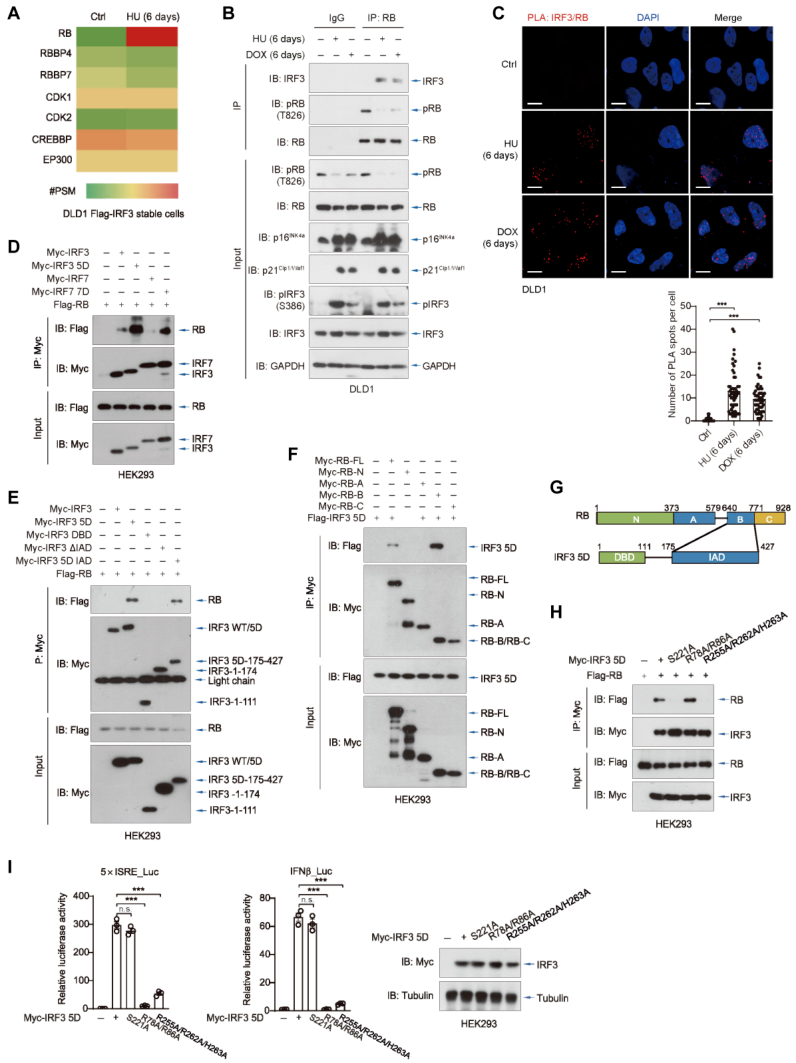 图 3 IRF3 直接与 RB 相互作用,RB 是细胞衰老的关键调节因子
图 3 IRF3 直接与 RB 相互作用,RB 是细胞衰老的关键调节因子4. IRF3 减弱 RB 过度磷酸化并启动细胞衰老
RB 在细胞周期调控中起着关键作用,特别是它与 E2F 家族和其他转录因子的相互作用。RB 在多个位点(如 CDK4 对 T826 和 CDK6 对 T82)的磷酸化,是其抑制和 E2Fs 产生相互作用的关键。缺乏这些抑制性磷酸化的 RB 突变体 (T821A/T826A,称为「活化 RB」) 对 E2F 蛋白具有高亲和力,显示出与拟磷酸化 IRF3 的强关联 (图 4A)。IRF3 敲除可阻止应激诱导的人胚胎成纤维细胞 MRC-5(图 4B) 和永生化 MEFs(图 4C) 中 T826 磷酸化-RB 的下调。将 IRF3 重新引入到 IRF3 KO 细胞中可恢复 DNA 损伤诱导的衰老过程中观察到的磷酸化-RB 水平的降低 (图 4D)。
此外,IRF3 S221A 突变体的 DLD1 IRF3 KO 细胞抑制 RB 过度磷酸化的能力减弱 (图 4E)。这些数据表明 IRF3 对 RB 低磷酸化的强大调节以及 IRF3 在衰老中的重要性。相比之下,使用 Tet-On 系统诱导表达 STING R281Q(STING 的组成活性形式),导致磷酸-RB 水平逐渐降低 (图 4F),细胞衰老增加 (图 4 G)。为进一步探索这种调节,研究人员在 A549 细胞中使用 STING 敏感系统,如 SA-β-Gal 染色所示,A549 细胞中的 IRF3 KO 抑制磷酸-RB 的减少 (图 4 H) 并阻止衰老的诱导 (图 4I)。
RB 磷酸化通常促进细胞周期进程,而其去磷酸化通过关联和抑制 E2F 转录因子导致细胞增殖停滞。集落形成实验显示,诱导 STING 表达的 A549 细胞中存在明显的生长停滞 (图 4J),细胞计数实验和 EdU 染色进一步证实这一点 (图 4K 和图 S4 H)。值得注意的是,在 STING-Flag Tet-On A549 细胞中,与 IRF3 阴性 KO 细胞相比,IRF3 的 KO 阻止这种增殖抑制 (图 4J-K)。这些数据表明,STING-TBK1-IRF3 轴控制细胞进入衰老,导致增殖停滞。
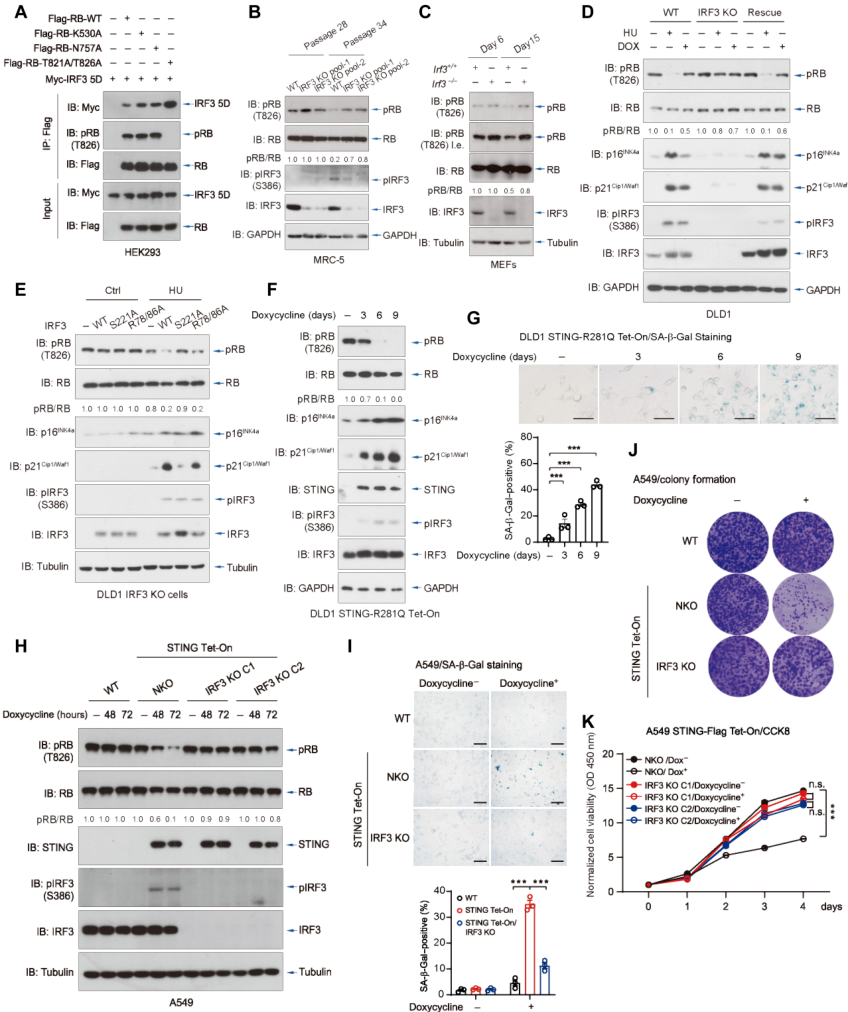 图 4 IRF3 减弱 RB 的过度磷酸化
图 4 IRF3 减弱 RB 的过度磷酸化5. IRF3- RB 相互作用阻止 CDK 介导的 RB 磷酸化,从而激活 RB
为充分了解 IRF3 如何激活 RB,研究人员生成表达各种形式 IRF3 的稳定 DLD1 细胞系,包括 WT、S221A 和 R78A/R86A。IRF3 S221A 预期不与 RB 相互作用 (图 5A-B),这与减少进入衰老相关,SA-β-Gal 染色 (图 5C) 和 SASP 水平 (图 S5A) 证明这一结果。然而,该突变体保留激活下游 IFN 信号的能力。这些观察结果强调 IRF3-RB 轴在对损伤的衰老调控中的重要性,而不依赖于 IRF3 的转录活性。
此外,研究人员使用体外激酶测定系统,分别表达和纯化 CDK4、CDK6、cyclin D1、RB 和 IRF35D 蛋白。在这个系统中,CDK4/6 在 cyclin D1 存在下,直接磷酸化 RB 的 T826 和 T821 位点,这一过程被 CDK4/6 抑制剂 palbociclib 抑制 (图 5D)。值得注意的是,IRF35D 的加入以剂量依赖的方式阻断 CDK4 介导的 RB 磷酸化,这表明 IRF3 在阻止 CDK4/6 介导的 RB 失活中起着至关重要的作用,也是 cGAS-STING-IRF3 信号传导诱导细胞衰老的关键机制。
为区分 IRF35D 是通过 RB-IRF3 相互作用影响 CDK4/6 激酶活性还是干扰 CDK4/6-RB 磷酸化,研究人员分析 CDK4 介导的另一种 CDK4 底物 Smad3 的磷酸化。CDK4 介导的 RB(而不是 Smad3) 磷酸化的选择性抑制 (图 5E) 强调 IRF3-RB 相互作用的重要性。与缺乏 RB 相互作用能力的突变体不同,IRF35D 破坏、RB-CDK4/6-cyclin D1 相互作用 (图 5F)。
这些结果提示 IRF3 通过与 RB 的相互作用阻止 CDK 介导的 RB 磷酸化的直接机制。接下来,研究人员评估 IRF3 在 RB-E2F 复合物形成中的作用。值得注意的是,IRF3 的活化形式极大地促进 RB 和 E2F1 之间的关联 (图 5 G),在 HU 诱导的衰老细胞中观察到内源性 E2F1 和 IRF3 与 RB 的相互作用 (图 5 H),证实内源性 RB-IRF3-E2F1 复合物在 DNA 损伤响应中的存在。
这些观察结果表明,cGAS-STING 诱导的干扰素反应和衰老是相互联系和相互增强的,可能是因为细胞微环境中复杂的相互作用。研究结果阐明 STING 诱导的细胞衰老启动的直接分子机制,涉及在细胞核中形成 IRF3-RB-E2F 复合物抑制 CDK 介导的 RB 磷酸化并干扰 E2F 介导的转录。
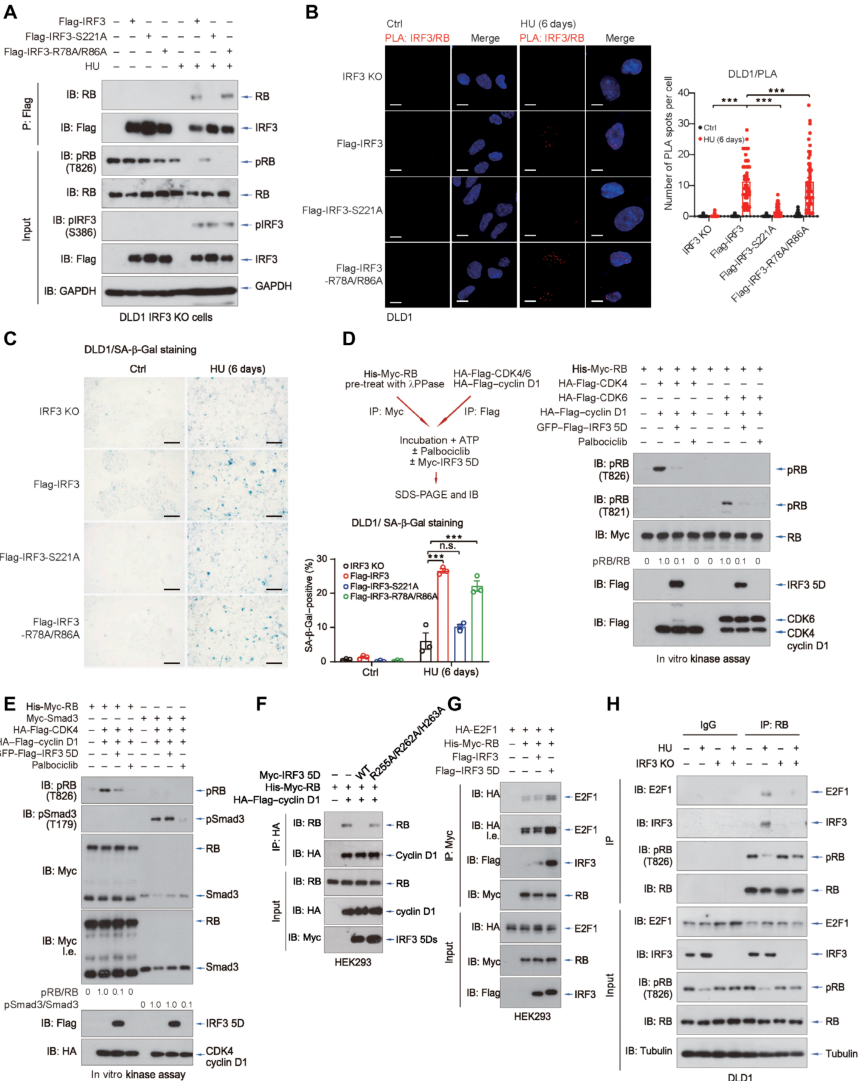 图 5 IRF3 通过减弱 CDK 诱导的 RB 磷酸化而激活 RB
图 5 IRF3 通过减弱 CDK 诱导的 RB 磷酸化而激活 RB6. IRF3 促进肝纤维化过程中 HSC 的衰老
先前的研究强调细胞衰老在减轻肝纤维化中的关键作用。为研究 STING-IRF3-RB 轴在这种情况下的生理影响,研究人员研究四氯化碳 (CCl4) 或胆管结扎 (BDL) 诱导的小鼠肝纤维化。在 CCl4 或 BDL 治疗后,小鼠肝脏中明显存在衰老细胞和胶原纤维 (图 6A-B),IRF3−/− 肝脏的细胞衰老明显减少,这一表型与 CDK4/6 抑制剂 Palbociclib 相反 (图 66A-B),表明 IRF3 在调节肝纤维化衰老中起关键作用。
天狼星红染色证实,在 CCl4 诱导的肝纤维化模型中,IRF3-/-小鼠的胶原沉积面积更大,胶原 mRNA 水平更高 (图 6C-D)。在 BDL 诱导的模型中也观察到相同的结果 (图 6E)。疾病参数,包括血清丙氨酸转氨酶 (ALT) 和天冬氨酸转氨酶 (AST) 水平在 BDL 诱导的肝纤维化中升高,在 IRF3−/− 小鼠中进一步升高 (图 6F)。这些发现提示 STING-IRF3-RB 轴通过促进细胞衰老来抑制肝纤维化。
为确定 SA-β-Gal 阳性的肝纤维化原代细胞类型,研究人员从 CCl4 治疗后的 WT 和 IRF3-/-小鼠肝脏中分离出原代肝细胞 (HCs) 和 NPCs。对衰老标记和 SASP 的分析表明,IRF3 缺失主要影响 NPCs 的衰老,而不是 HCs(图 6 G)。在 CCl4 诱导后,WT 小鼠的原发性 NPCs 中发现 IRF3 磷酸化,在 IRF3 KO NPCs 中观察到磷酸化-RB 水平升高 (图 6 H)。NPCs 的 cGAS 和 STING mRNA 和蛋白水平高于 HCs(图 6 H-I),这说明在肝纤维化过程中,NPCs 的 IRF3 激活增强,衰老更明显。
免疫荧光分析显示超过一半的 HSC 表达衰老标记 p21Cip1/Waf1(图 6J)。此外,IRF3−/− 小鼠的 HSC 细胞衰老减少,Palbociclib 治疗增加 IRF3 KO 小鼠的 p21+HSC 水平 (图 6J),与 SA-β-Gal 染色结果相同 (图 6B)。这些观察结果支持 IRF3-RB 复合物在抑制 HSC 驱动的肝纤维化中的关键作用,并暗示 CDK4/6 抑制可能是纤维化性肝病的一种有希望的治疗方法。
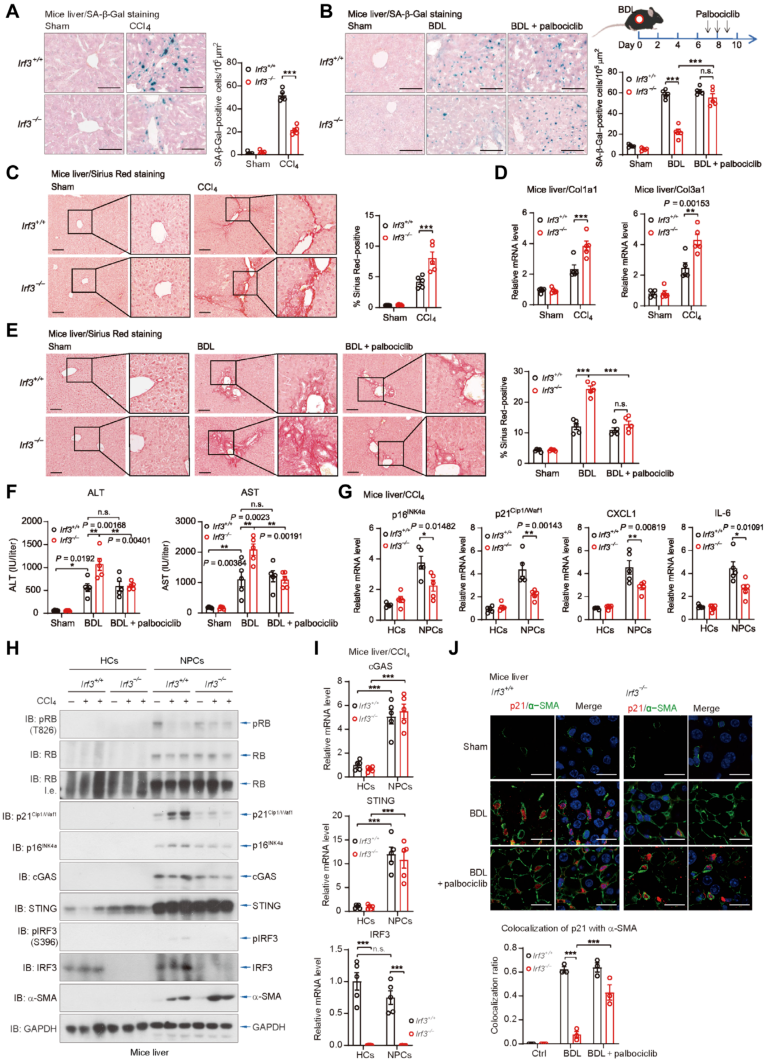 图 6 IRF3- RB 轴调节肝纤维化过程中的衰老
图 6 IRF3- RB 轴调节肝纤维化过程中的衰老7. STING- IRF3- RB 轴通过 HSC 衰老减少肝纤维化
为探索 STING-IRF3-RB 轴在肝纤维化过程中调节 HSC 细胞衰老中的体内作用,研究人员使用 HSC 特异性启动子驱动的腺相关病毒血清型-8(AAV8)-胶质纤维酸性蛋白 (GFAP)(启动子) 增强的绿色荧光蛋白 (EGFP)-cre 选择性地删除 Irf3flox/flox 小鼠 HSC 中的 IRF3(图 7A)。通过增加造血干细胞中 Cre mRNA 和 EGFP 的表达 (图 7B) 以及分离的造血干细胞中 IRF3 蛋白水平的降低 (图 7C) 证实靶向缺失。
经 CCl4 处理后,在造血干细胞中观察到 IRF3 活化和 RB 低磷酸化 (图 7C),靶向删除 HSC 中的 IRF3 导致衰老表型显著减少,这可以从持续的 RB 过度磷酸化 (图 7C),衰老标记物如 IL-6 和 p21Cip1/Waf1(图 7D) 以及衰老细胞减少 (图 7E) 中看出。此外,在 CCl4 诱导的纤维化过程中,造血干细胞中 IRF3 的选择性缺失导致肝脏中胶原纤维聚集增加 (图 7F) 和胶原相关基因表达升高 (图 7 G)。
在 WT 和条件 IRF3 KO 小鼠之间检测到胆管和血管附近的 NPCs 明显增加 (图 7 H),但肝脏中的炎症因子没有增加 (图 7I)。这些发现与 IRF3 KO 小鼠 BDL 模型的结果一致,强调 cGAS-STING-IRF3-RB 信号在 HSC 介导的肝纤维化中起关键抑制作用。
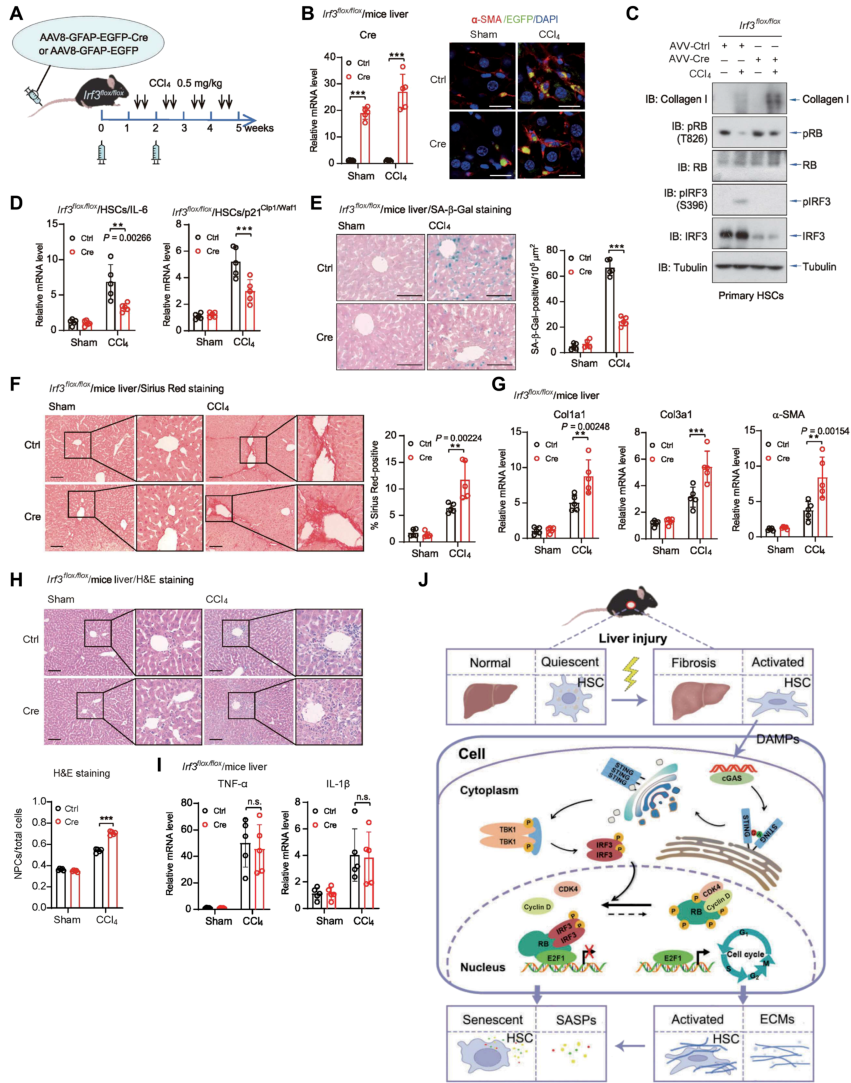 图 7 在 HSC 中选择性删除 IRF3 可减缓 HSC 衰老并促进肝纤维化
图 7 在 HSC 中选择性删除 IRF3 可减缓 HSC 衰老并促进肝纤维化文章小结
本研究发现 IRF3 通过与 RB 互作形成 IRF3-RB-E2F 复合体,从而阻碍 CDK4/6-cyclinD1-RB 复合体的形成,因此保持 RB 在低磷酸化的活化状态以阻滞细胞周期,从而诱导细胞进入衰老状态。总的来说,这篇文章阐明 cGAS-STING-IRF3-RB 信号轴这一非经典的调控细胞衰老信号路径,并揭示其促进肝星状细胞衰老以减缓肝纤维化进展的生理和病理功能。这些新发现明确提出天然免疫机制调控器官纤维化的疾病和细胞类型依赖性,为肝纤维化的治疗提供了新的理论与实验依据。
本文及图片来源于好本子,作者转载