最新研究成果吧!

电压门控钙离子通道 Cav1.2 是大脑、心肌和平滑肌L型钙通道的主要亚型,对许多生理与神经活动至关重要,如心肌和平滑肌收缩,以及学习和记忆功能等。Cav1.2 功能异常增强与蒂莫西综合症有关,这是一种罕见的常染色体显性障碍,病理表现为心肌病、心律失常、蹼趾和自闭症谱系障碍等。Cav1.2 是多种临床常用药物和天然毒素的作用靶标。
文章题为「Structural basis for human Cav1.2 inhibition by multiple drugs and the neurotoxin calciseptine」(《多种药物及神经毒素 calciseptine 抑制人源钙离子通道蛋白 Cav1.2 的分子机制》)。研究揭示了自由状态、多种药物结合、多肽毒素结合的钙离子通道 Cav1.2 的高分辨结构。
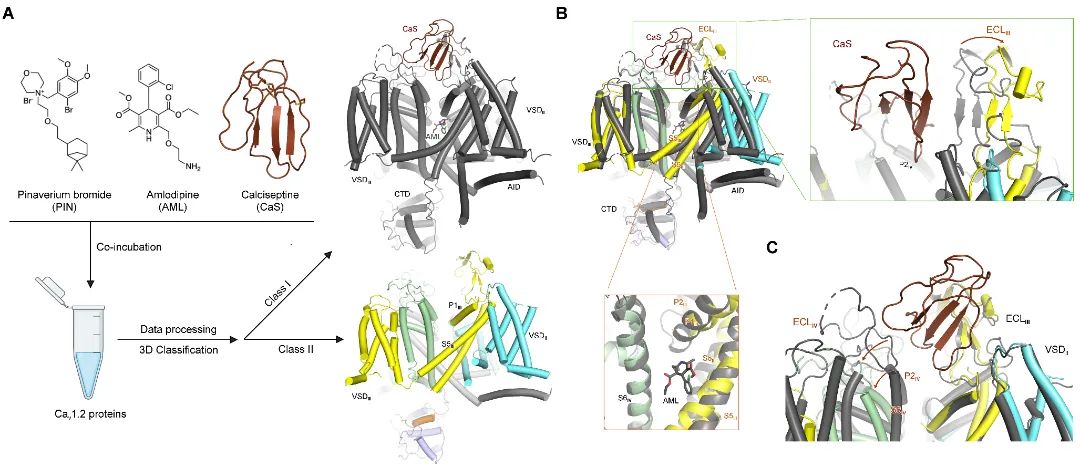 ▲Calciseptine、匹维溴铵(Pinaverium)稳定Cav1.2蛋白两个完全不同的失活构象
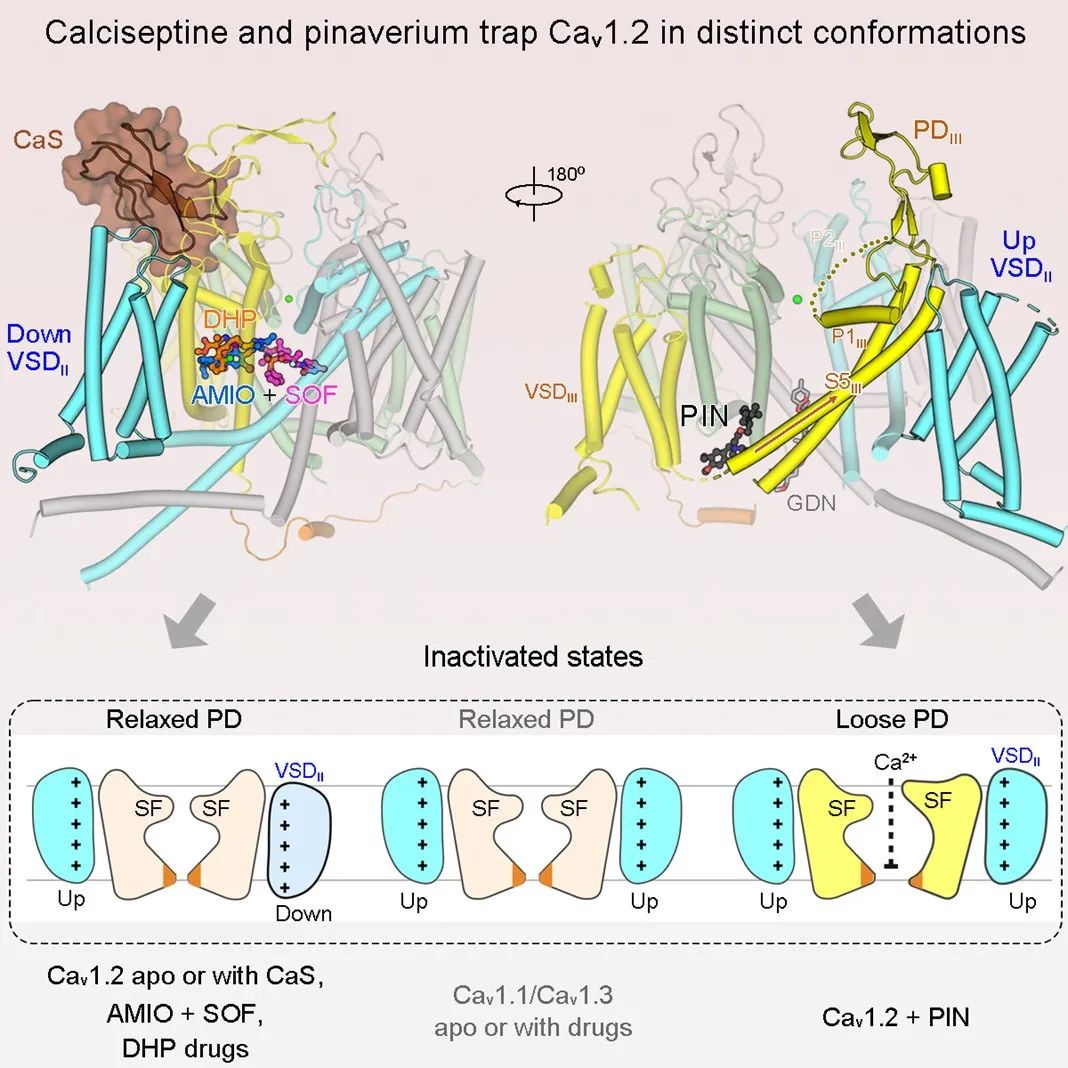
▲Calciseptine、匹维溴铵(Pinaverium)稳定Cav1.2蛋白两个完全不同的失活构象无论是自由形式,还是与黑曼巴蛇毒素 calciseptine、氨氯地平,胺碘酮与索非布韦结合,Cav1.2 通道都呈现出一致的失活构象。在解析多种药物调控 Cav1.2 作用机制的过程中,作者获得了三个重要的非预期发现:
第一
尽管 Cav1.2 与 Cav1.3 同属于 L 型钙离子通道,在功能及序列上高度同源,但 Cav1.2 在部分结构特性上更接近于神经钙离子通道 Cav2.2/Cav2.3。具体而言,Cav1.2,Cav2.2,Cav2.3 的电压感受结构域 II(VSDII)处于 down 构象;Cav1.1,Cav1.3 的 VSDII 则处于 up 构象;
第二
该研究解析了眼镜蛇毒素 calciseptine 致死的分子机制,颠覆了以往对动物毒素调控离子通道功能的认知。经典的动物毒素结合模式一般是通过结合在在离子孔结构域阻碍离子运输,或者结合在电压感受结构域变构调控离子通道功能。在本工作中,Calciseptine 结合在 Cav1.2 离子孔外周的肩膀区域,这种崭新的结合模式稳定了 Cav1.2 通道失活状态的构象,导致蛋白功能抑制。毒素及蛋白定点突变电生理研究进一步验证了该结合模式;
第三
该研究在解析胃肠道解痉剂匹维溴铵调控机制时,发现了 Cav1.2 通道的全新失活构象。在该构象中,VSDII 呈现 up 状态,离子孔扩大,选择性滤器(SF)构象改变。与此同时,重复单元 III 的 S4-S5 与 S5 两个 α 螺旋元件融合成单个螺旋,导致细胞内孔(Intracellular gate)变宽。除匹维溴铵外,氨氯地平等其他药物分子不能结合该构象。通过分子动力学模拟证实,这个孔道结构域变大的构象仍不能通透钙离子,通道蛋白处于失活状态。
武汉大学药学院高帅教授、深圳医学科学院院长颜宁教授、北京大学宋晨研究员为该文章共同通讯作者,武汉大学药学院高帅教授、姚霞教授、清华大学陈姣凤博士为该文章共同第一作者。武汉大学药学院为文章第一完成单位。清华大学化学系刘磊教授、圣约翰大学于勇教授为该工作提供了重要帮助。感谢武汉大学泰康生命医学中心提供科研经费支持。这是高帅教授、姚霞教授在 Nature(2021)、Cell Research(2022)、Cell(2022)、Nature Communications(2022)杂志发表钙离子通道镇痛药物齐考诺肽、抗晕动症药物桂利嗪,丙肝神药索非布韦副反应作用机制后,在该领域的又一系统性、突破性进展,为钙离子通道蛋白新型靶向药物研发奠定了重要的理论基础。

后排 姚霞 孙晓钰 刘俊午 朱远载 高帅
前排 黄雨馨 潘登 姜巧云 李芊 赵白雪
(从左至右)
踏平坎坷成大道越是艰险越向前武大科研人播撒创新之种
迈出坚实步伐在无涯学海里厚积薄发在无止境的探索道路上勇往直前