导读
增殖细胞核抗原(PCNA)是存在于所有真核细胞中的一种进化保守的多面蛋白,在 DNA 合成和 DNA 修复中发挥着关键作用。PCNA 围绕 DNA 形成一个同型三聚体环状结构,作为复制体的中心「枢纽」,能够锚定许多参与复制和修复途径的蛋白质。一直以来,PCNA 被广泛用作肿瘤进展的标记物。不过最近的研究表明,PCNA 可以发挥有丝分裂作用,通过细胞外囊泡远程恢复衰老细胞。
DNA 复制压力是癌细胞的一个标志。利用这种与癌症相关的特征,通过引入进一步的 DNA 损伤可以导致癌细胞的死亡,因此它被用作主要的抗癌治疗策略。与癌细胞相关的一种独特的 PCNA 亚型的鉴定,可能为新的化疗药物的开发开辟了一条新的途径。前期的研究已经发现了几个靶向 PCNA 的分子,包括小分子和基于肽的分子,这表明直接靶向 PCNA 治疗癌症可能是一种可行的方法。
2023 年 8 月 1 日,,美国最大的癌症研究和治疗组织之一——希望之城贝克曼研究所等单位的研究人员在 Cell Chemical Biology 杂志发表了题为 Small molecule targeting of transcription-replication conflict for selective chemotherapy 的文章,通过合理的药物设计方法,他们发现了一种小分子 PCNA 抑制剂 AOH1996,它可以在临床前研究中选择性地杀死所有类型的癌细胞。
在机制层面,他们发现 AOH1996 增强了 PCNA 与 RNA 聚合酶 II 最大亚基 RPB1 之间的相互作用,并将 PCNA 从转录活跃的染色质区解离,同时以转录依赖的方式诱导 DNA 双链断裂。AOH1996 能够作为抑制肿瘤生长的单一疗法或联合治疗,并且没有明显的副作用。在动物研究中,它几乎完全抑制异种移植瘤的生长,并使它们对拓扑异构酶抑制敏感。
本研究的结果首次证明了 PCNA 和 RBP1 相互作用产生了癌症选择性易感性,这可以在临床前模型中很容易观察到。AOH1996 作为一种化学工具的潜在用途,进一步定义细胞中的转录-复制冲突(TRCs),并清楚地证明了 AOH1996 作为单一疗法时的治疗潜力,以及它与现有的化疗联合使用时的治疗潜力。
 图片来源:Cell Chemical Biology
图片来源:Cell Chemical Biology主要研究内容
AOH1996 可靶向 PCNA
前期,该团队报道过一种 PCNA 配体 ——AOH1160,它可以靶向 PCNA 的癌症特异性 L126-Y133 区域,并对癌细胞具有选择性毒性。在本研究中,他们基于 PCNA 与其潜在配体之间的相互作用,通过使用建模工具,设计并合成了大约 70 种 AOH1160 类似物,并从中鉴定了一种类似物 AOH1160-1LE,预测其溶解度显著增加;鉴定到的另一种类似物为 AOH1996,这是通过在末端苯基环的侧位上添加甲氧基得到的。为了证实 AOH1160-1LE、AOH1996 与 PCNA 的结合,他们进行了热变性分析,结果发现他们与 PCNA 的稳定相互作用。
在 PCNA 同型三聚体的链 A 和链 B 中,中心的 AOH1160-1LE 分子与 PIP 盒结合腔近似垂直于结合腔。在 AOH1996-1LE(AOH1996 类似物)晶体结构中也观察到三个结合分子,并容纳了额外的甲氧基基团,使 AOH1996-1LE 的结合模式与 AOH1160-1LE 的结合模式相似。
 图片来源:Cell Chemical Biology
图片来源:Cell Chemical BiologyAOH1996 的优良治疗特性
基于 AOH1996 的靶标(caPCNA)在癌细胞中的广泛表达,研究人员在 70 多个癌细胞系和几种正常对照细胞中进行了检测。结果发现 AOH1996 可以选择性地杀死癌细胞;相比之下,AOH1996 对非恶性细胞没有明显的毒性。
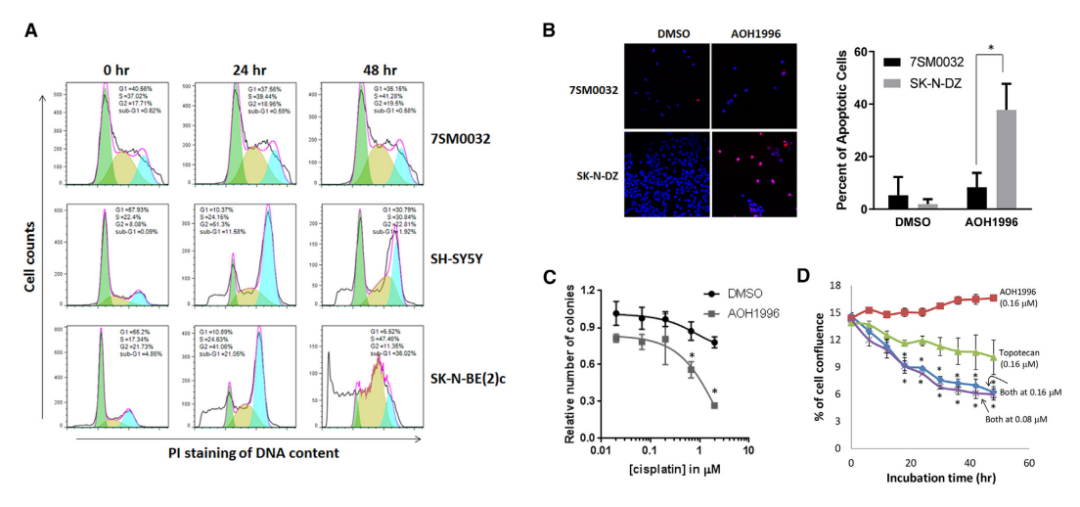
AOH1996 诱导了细胞周期谱的实质性变化,表明癌细胞中 G2/M 或 S 期停滞。此外,通过流式细胞术和 TUNEL 检测的阳性反应,表明 AOH1996 在癌细胞中诱导了细胞凋亡;但 AOH1996 不会显著改变非恶性神经嵴干细胞的细胞周期,也不会诱导其凋亡。
此外,AOH1996 还增加了癌细胞对包括顺铂在内的基因毒性药物的敏感性。在 AOH1996 和拓扑替康之间也观察到了类似的协同作用,拓扑替康是一种拓扑异构酶 I 抑制剂,可以阻止拓扑异构酶 I 重新连接被切割的 DNA 链,从而在 DNA 复制过程中导致双 DNA 链断裂(DSB)。
 图片来源:Cell Chemical Biology
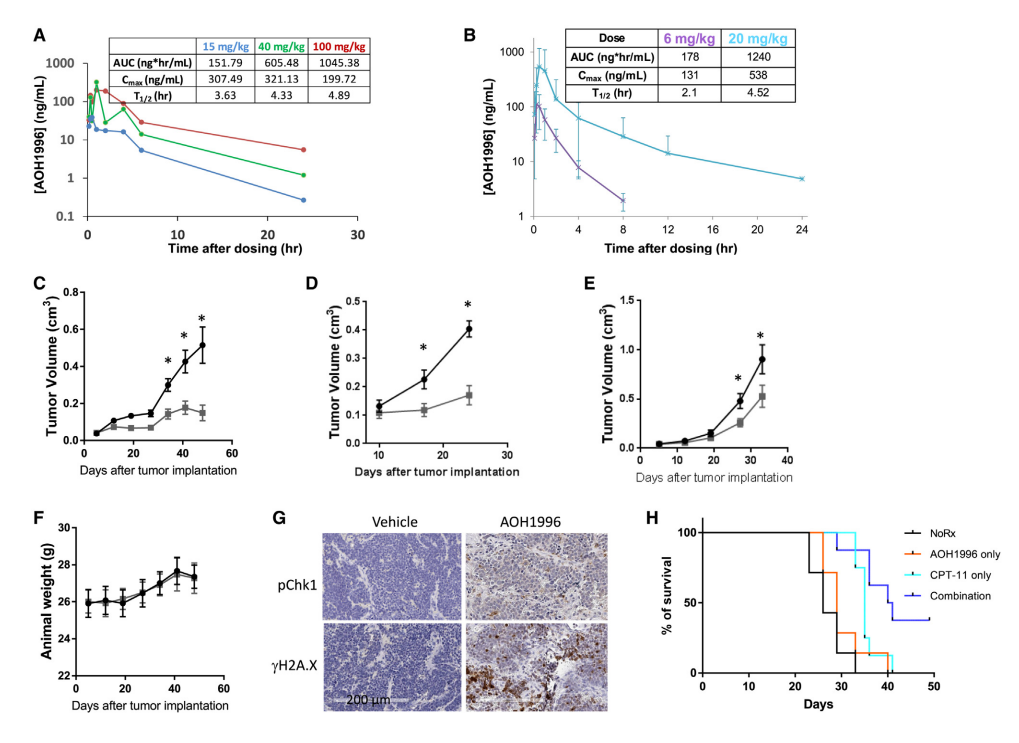
图片来源:Cell Chemical Biology随后,他们检测了 AOH1996 在小鼠体内的抗癌活性,小鼠体内的肿瘤来源于神经母细胞瘤或乳腺或小细胞肺癌细胞。与对照组相比,每日 AOH1996 治疗显著降低了动物的肿瘤负担,并且 AOH1996 没有造成任何死亡或显著体重下降。此外,在小鼠实验中,AOH1996 的无观察不良反应水平(NOAEL)为 250 mg/kg/剂量,每日两次。
为了确定药效学标记物,他们使用免疫组化方法分析从使用 AOH1996 或只使用载体的小鼠身上采集异种移植瘤。局灶性 gH2A.X 染色和 phospho-Chk1 仅在 AOH1996 治疗的肿瘤中可见。总的来说,AOH1996 治疗小鼠的肿瘤密度低于对照组小鼠。这些结果与 AOH1996 在癌细胞中引起 DSB 和 G2/M 阻滞的观察一致,并证明了 gH2A.X 染色和 phospho-Chk1 可以作为其临床药效学标志物。
 图片来源:Cell Chemical Biology
图片来源:Cell Chemical Biology调节 PCNA 与转录机制的相互作用
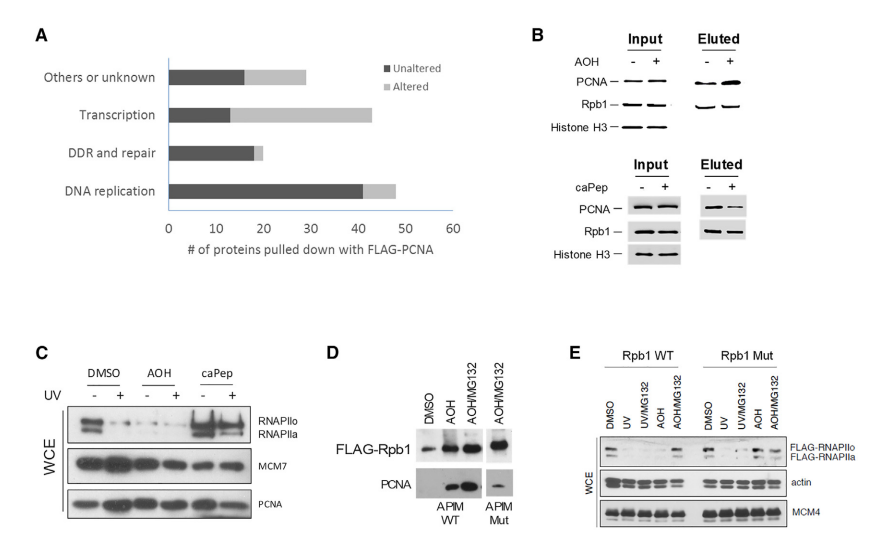
PCNA 与其结合伴侣相互作用的免疫沉淀和质谱分析显示,与染色质结合的 PCNA 相关的超过 50% 的蛋白被 AOH1996 改变,这些蛋白是细胞转录过程的组成部分。进一步的免疫沉淀研究发现,AOH1996 增强了癌细胞中 PCNA 和 RPB1 之间的相互作用,并使 RPB1 减少。后续的实验还表明 AOH1996 增加了转录-复制冲突(TRC),增强了 RPB1 与 PCNA 之间的相互作用。通过检测全细胞提取物中外源表达 RPB1 的水平,他们发现 AOH1996 以蛋白酶体依赖的方式引起野生型 RPB1 的降解。
 图片来源:Cell Chemical Biology
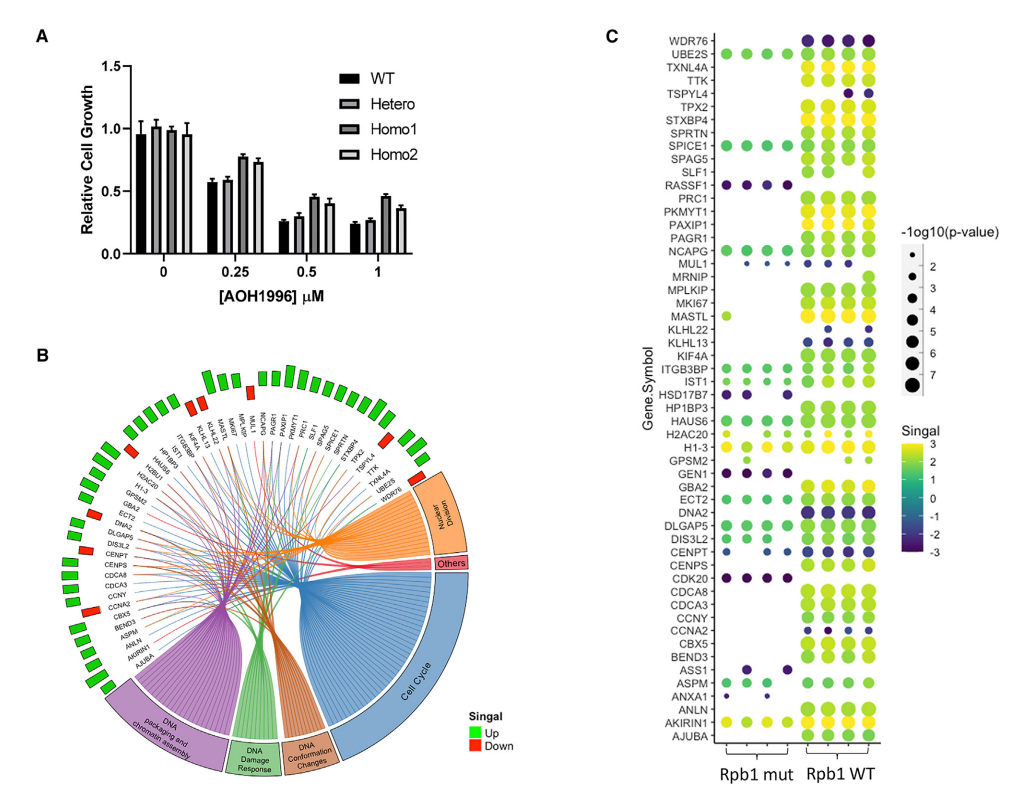
图片来源:Cell Chemical Biology他们还利用 CRISPR 在人神经母细胞瘤细胞系 SK-N-AS 中将 RPB1-418 位点的酪氨酸突变为丙氨酸。Y418A 突变等位基因的纯合子细胞对 AOH1996 生长抑制的敏感性显著低于亲本细胞。质谱和基因本体(GO)富集分析表明,在 AOH1996 处理后的两个细胞系中,参与细胞周期调控和 DNA 复制和修复的蛋白占了 54 个差异蛋白中的 49 个,这些蛋白的水平至少改变了 2 倍,且具有统计学意义。AOH1996 处理引起的大部分变化在亲本细胞中要比在 RBP1 突变细胞中高得多,再次表明 AOH1996 发挥作用,至少部分是通过调节 PCNA 与 RPB1 的相互作用。
 图片来源:Cell Chemical Biology
图片来源:Cell Chemical Biology结语
总的来说,该研究开发了一种靶向 PCNA(增殖细胞核抗原)的抗癌小分子药物 AOH1996。临床前研究结果显示,在 70 多个癌细胞系和几组正常细胞中,AOH1996 可以选择性地杀死所有类型的癌细胞;且 AOH1996 对正常细胞没有明显的毒性。
该研究证明了这种先导化合物的治疗潜力,抑制转录-复制冲突的解决可能为选择性杀死癌细胞开辟了一种新的治疗途径。据悉,该药物已进入 I 期临床试验。
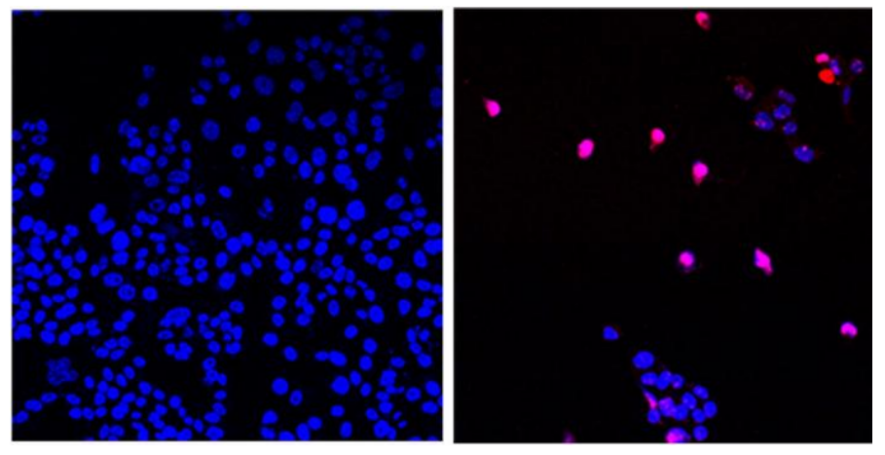 未经处理的癌细胞(左)和用 AOH1996 处理的癌细胞(右)正在经历程序性细胞死亡(紫色)(图片来源:City of Hope)
未经处理的癌细胞(左)和用 AOH1996 处理的癌细胞(右)正在经历程序性细胞死亡(紫色)(图片来源:City of Hope)本研究通讯作者 Linda H. Malkas 教授说到:「PCNA 就像一个主要的航空枢纽,包含多个飞机登机口。数据表明,PCNA 在癌细胞中发生了独特的改变,这一事实允许我们设计一种只针对癌细胞中 PCNA 形式的药物。我们的抗癌药物就像一场暴风雪,关闭了一个关键的航空枢纽,使所有携带癌细胞的航班停飞。我们目前的结果很令人兴奋,在细胞和动物模型中,AOH1996 可以作为单一疗法或联合疗法抑制肿瘤生长而不产生毒性。这种实验性化疗药物目前正在希望之城进行 I 期临床试验。」
该研究第一作者 Long Gu 说:「从来没有人把 PCNA 作为一种治疗手段,因为它被视为『无药可治』,但很明显,希望之城能够针对具有挑战性的蛋白质靶点开发出一种实验性药物。我们发现,PCNA 是癌细胞中核酸复制错误增加的潜在原因之一。现在我们知道了问题所在,并能够抑制它,我们将更深入地了解过程,以开发更个性化、更有针对性的癌症药物。」
值得提醒的是,尽管该药有着如此强大的功能,并被称为「超级抗癌药」,但目前该药仍处于临床前研究。
8 月 3 日,哈尔滨血液病肿瘤研究所所长、中国临床肿瘤学会(CSCO)创始人及监事长马军教授在采访时表示:「从临床来看,一款好的肿瘤药要看其有效性和安全性,目前 AOH1996 的研究结果来自临床前期,虽然带来了肿瘤治疗的新希望,但仍需要二三期临床试验诸多环节的证实。目前来看,肿瘤治疗没有『神药』。」
深圳市第三人民医院院长卢洪洲也提到:「AOH1996 虽然在细胞模型和动物模型的临床前研究中证实其安全性和有效性,但是该药物是否能够在后续的 I/II/III 期临床试验达到预设研究终点,是否能够表现出优异的安全性和有效性,我们还需持谨慎态度,需要等临床试验数据发布再行判断。」
图片来源:City of Hope参考文献:1. Gu et al., Small molecule targeting of transcription-replication conflict for selective chemotherapy, Cell Chemical Biology (2023).2. Hanahan, D., and Weinberg, R.A. (2011). Hallmarks of cancer: the next generation. Cell 144, 646–674.3. Lei, Q., et al. (2021). Extracellular vesicles deposit PCNA to rejuvenate aged bone marrow-derived mesenchymal stem cells and slow age-related degeneration. Sci. Transl. Med. 13, eaaz8697.
