
此时此刻,数十亿个 B 细胞和 T 细胞正在你的血液中循环,挤满了你的骨髓、脾脏和胸腺。据估计,B 细胞的总数多达 100 亿个,而 T 细胞也有 2,500 万至 10 亿个[1,2]。
然而,寻找抗原特异性的 B 细胞和 T 细胞或者突破性的免疫疗法,无异于大海捞针。许多研究人员历经数周甚至数月的艰苦实验,终于获得了一些抗原特异性候选物,但这些候选物却往往无法揭示对治疗有帮助的罕见克隆型。
在传统方法无能为力的地方,BEAM(Barcode Enabled Antigen Mapping)脱颖而出,这正是我们新开发的抗原特异性 B 细胞和 T 细胞发现流程。
BEAM 的出现让科学家们能够以 Chromium 单细胞免疫分析解决方案为基础,通过多重抗原筛选流程捕获抗原特异性 B 细胞和 T 细胞的高分辨率细胞图谱。仅需一周时间,研究人员就能够生成数十个至数百个高质量的抗原特异性候选物,以无与伦比的速度实现细胞表征。如今,学术界和转化研究人员都有一个完整的端对端解决方案,能够为时间紧迫的患者挖掘强效的抗体,揭示新的癌症免疫疗法,并提供疫苗开发的信息。
本文将带您深入了解发现抗原特异性 B 细胞和 T 细胞可能面临的各种挑战,BEAM 背后的科学,以及如何利用它来实现下一个重大的治疗突破。
释放 B 细胞和 T 细胞的治疗潜能
B 细胞和 T 细胞在适应性免疫系统中发挥着至关重要的作用,可识别被身体定义为外源物的分子(又称为抗原),随后引发清除这些分子及其来源的病原体(比如病毒或细菌)的一系列事件。这种功能是通过 B 细胞受体和 T 细胞受体识别抗原来实现的。
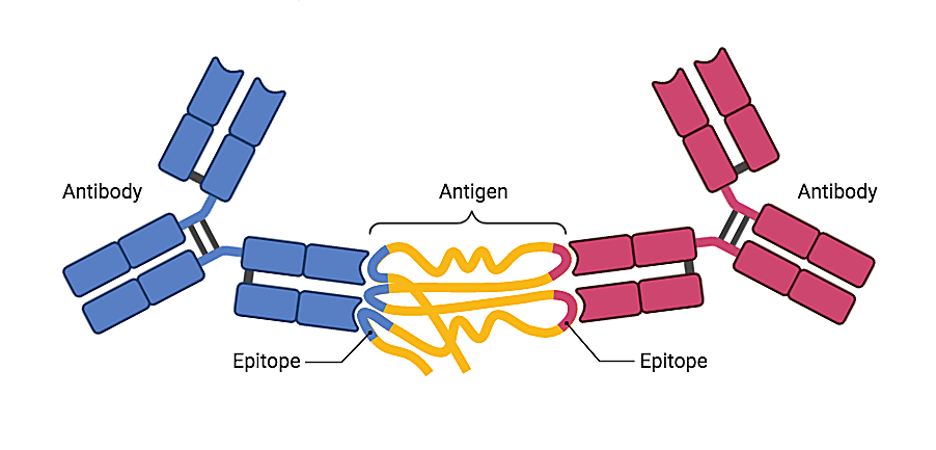
抗体(BCR)识别抗原。图片来源:https://app.biorender.com/biorender-templates/t-5f4fb6cc3b02b700b74df63f-antigen-recognition-by-antibodies. BioRender (2022).
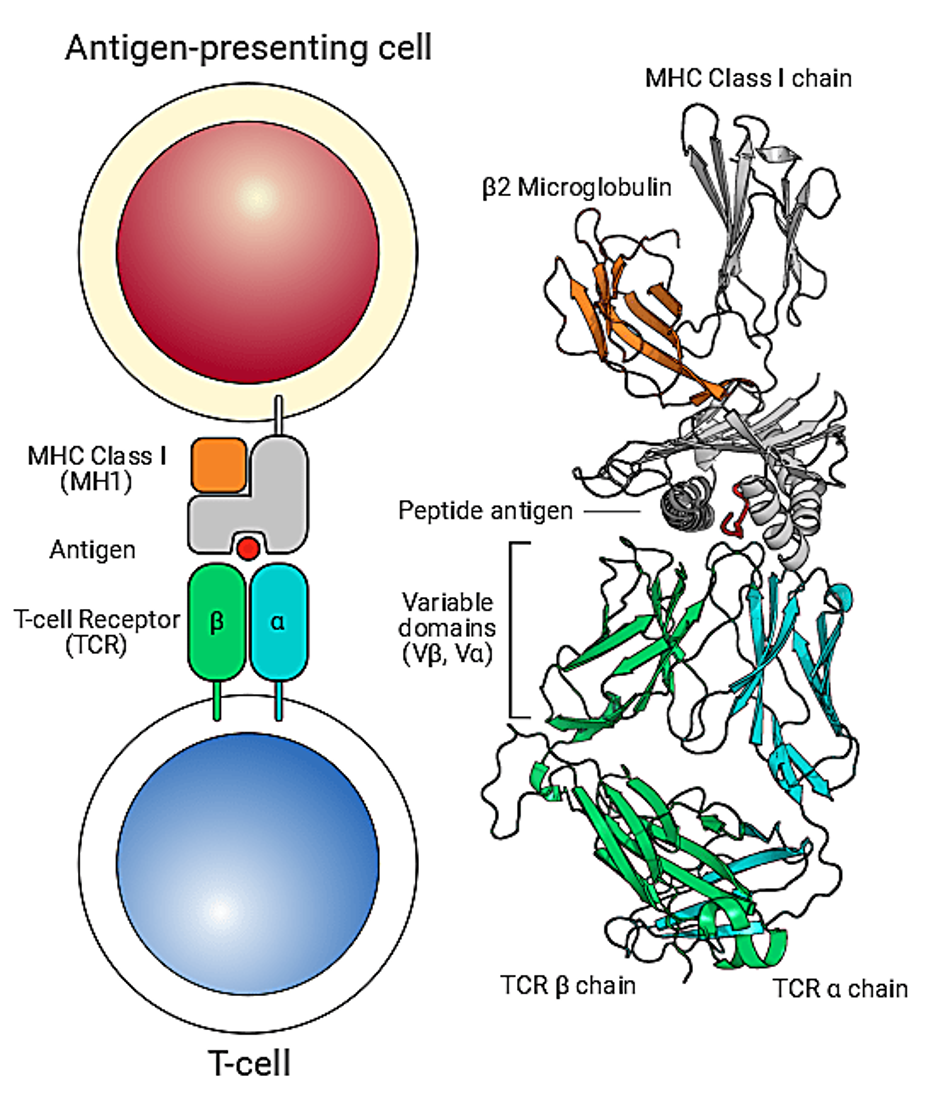
T 细胞依赖其表面受体来识别并结合外源抗原以及与疾病相关的抗原,这些抗原以肽段分子的形式出现,由固有免疫细胞(如树突状细胞及其他抗原呈递细胞)呈递。这是 TCR 识别抗原所需核心组分的示意图。图片来源:Leem et al., Nucleic Acids Res. (2018), 46, D406-D412. (BY CC 4.0)
人体内现有的 BCR/TCR 库的整体多样性被称为功能性适应性免疫组库。其中,功能性是关键。当受体与抗原结合时,B 细胞和 T 细胞被选派来执行其免疫功能。B 细胞释放抗原反应性抗体来中和病原体,杀伤性 T 细胞则开始摧毁患病细胞——但不幸的是,若出现功能障碍,那些识别自身抗原的 B 细胞和 T 细胞会驱动有害的自身免疫反应。
BCR 和 TCR 上带有可变的抗原结合区,由可重排或突变的 V(D)J 基因序列编码,产生了数量惊人的抗原反应性受体组合。人们在计算独特 V(D)J 组合的可能数量时发现,理论上有 1018 种可能的 BCR[3] 和 1015 种可能的 TCR[4]。
适应性免疫系统产生的 B 细胞和 T 细胞克隆型也超出了人体的处理能力——1015 个单个 T 细胞重达 500 公斤(相当于 1,100 多磅)[4]。这些看似无限的受体能够与种类繁多的抗原相结合并支持其清除,从而改变治疗研究。
研究人员已经发现了一些能够转化为强大疗法的受体-抗原关系。PD1 单克隆抗体是一种适用于多种癌症的高效疗法,它与 T 细胞上的 PD-1 受体结合,阻断免疫抑制信号,并激活 T 细胞的抗肿瘤功能[5]。CAR T 细胞疗法也用于某些癌症的治疗,并在狼疮等自身免疫性疾病的治疗中表现出希望[6]。
然而,这些疗法只对部分患者有效。此外,除了癌症、自身免疫和传染病外,我们仍在研究有多少种疾病实际上是通过免疫细胞介导的或受到其影响,包括神经退行性疾病[7]。如果研究人员能够深入挖掘功能性适应性免疫组库,他们将释放出前所未有的治疗潜力。
抗原特异性 B 细胞和 T 细胞的发现困难重重
那么,我们如何才能系统地了解和利用功能性适应性免疫组库,以解决疾病和医学中的基本问题?这并非易事。
将抗原与其对应的 BCR/TCR 相匹配一直是很困难的。抗体发现的常用方法,如杂交瘤技术和噬菌体展示等,通常需要数周甚至数月的艰苦实验。基于杂交瘤的方法往往只能针对一种抗原产生 1~3 个扩增克隆,并需要 8~12 周的进一步验证,总共需要 6~9 个月的实验[8]。
这些方法还对研究人员使用的样本有所限制。例如,杂交瘤是骨髓瘤细胞与脾细胞融合后的产物[8],但治疗上有用的 BCR 可在血液样本、骨髓和淋巴结穿刺液等样本中找到。
抗原特异性 T 细胞的发现也同样具有挑战性,这主要是由于 TCR 结合的要求高以及细胞分离的实际考虑。T 细胞有着非常特殊的结合要求:它们只喜欢与完美固定装置(被称为主要组织相容性复合物 MHC)上展示的抗原相结合,MHC 出现在抗原呈递细胞的表面。然而,目前很难开发出稳定的肽段-MHC 复合物,对样本中抗原特异性 T 细胞进行标记和分离——因为 MHC 分子很大,容易分解,这使得自行开发稳定化操作变得艰难,也不可靠。
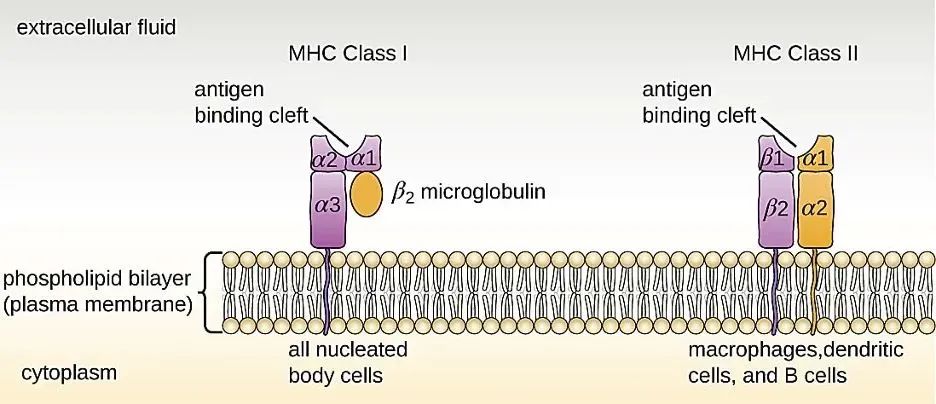
MHC I 类分子存在于所有有核的体细胞上,而 MHC II 类分子存在于巨噬细胞、树突状细胞和 B 细胞(与 MHC I 类分子一起)上。MHC I 类分子的抗原结合凹槽由 α1 和 α2 结构域组成。MHC II 类分子的抗原结合凹槽由 α1 和 β1 结构域组成。图片来源:OpenStax Microbiology。
具有与治疗相关的抗原特异性的 T 细胞往往只占众多类型的 T 细胞中的一小部分。研究人员经常采用基于荧光的分选方法来鉴定和收集样本中的抗原特异性 T 细胞,但这种方法远谈不上完美。由于标记肽段-MHC 分子的荧光基团数量有限,他们可能会错过稀有的抗原反应性 T 细胞群。此外,现有方法只能提供样本中抗原特异性 T 细胞的数量,因此对 T 细胞的状态或功能以及更大的免疫应答的了解有限。
凭借传统的抗体发现和抗原特异性 T 细胞分离方法。研究人员已经取得了重要的免疫治疗成果,但这个过程仍然像大海捞针。他们需要更快速、更可靠的方法来表征免疫细胞表型和抗原特异性,并解析稀有的克隆型,而不是像以往那样从有限的兼容样本中产生极少的抗原特异性候选物。
BEAM 如何帮助人们鉴定抗原特异性克隆型
为了克服阻碍目前的抗原特异性 B 细胞和 T 细胞发现流程的技术挑战,加速学术研究和治疗应用,我们开发出 BEAM 技术。 BEAM 是一种多重抗原筛选流程,能够快速发现抗原特异性的 B 细胞(BEAM-Ab)和 T 细胞(BEAM-T)克隆型。它以成熟的 Chromium 单细胞免疫分析方案为基础,让研究人员能够获得全面的抗原特异性细胞图谱,包括来自同一个单细胞的全长配对 V(D)J 序列、基因表达和细胞表面蛋白。 |
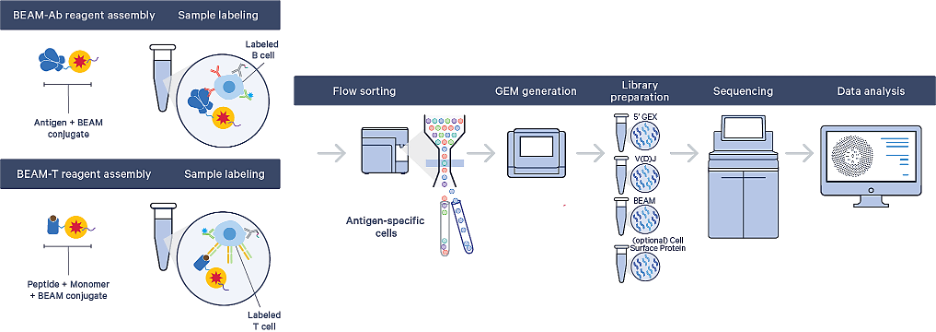
BEAM 流程从您感兴趣的抗原开始:研究人员在为期一周的单次实验中筛选数十万个 B 细胞或 T 细胞对多达 15 种抗原及 1 种对照的结合特异性。这意味着您可从同一个样本中生成数十个至数百个抗原特异性候选物——包括各种兼容的样本,如 PBMC、脾细胞、淋巴结穿刺液以及富集的 B 细胞或 T 细胞。
BEAM 使得从复杂样本中分离抗原特异性的 B 细胞和 T 细胞也变得更加轻松。研究人员能够自信地鉴定稀有的克隆型,并最大限度减少细胞损失,因为抗原与带有独特条形码的 BEAM 偶联物(包含 PE 荧光标记)相偶联。分离染色后的抗原特异性克隆型的流式分选步骤只是简单地检查荧光,而不是对有限的参数进行多色分析。 拥有稳定的肽段-MHC 复合物也不再是问题。BEAM-T 试剂组装物包含了成套的定制可加载的 MHC 单体,让研究人员能够将他们感兴趣的抗原肽段加载到空的单体上,然后对 T 细胞进行染色。这种方法带来了灵活性,可从任何供应商处设计和采购肽段。 BEAM 流程还包含易用的数据分析和可视化软件,可用来探索和解释抗原与克隆型之间的关系。通过比较感兴趣抗原相对于对照抗原的 UMI 计数来计算抗原特异性评分,可鉴定抗原特异性克隆型。 BEAM 流程从用户提供的抗原开始,首先用 10x Genomics BEAM 试剂在抗原上添加条形码,然后用带有条形码的抗原对 B 细胞或 T 细胞进行染色,再通过流式分选进行富集。之后在样本上开展正常的文库制备和测序步骤。(注:BEAM-Ab 和 BEAM-T 是利用独特的试剂在不同的流程中开展的。) |
接下来的部分,我们将深入探讨 BEAM 如何简化抗原特异性克隆型发现实验,以及它如何应用于真实的研究案例——从鉴定癌症新抗原特异性的 TCR,到调查和统计 COVID-19 感染后免疫图谱中的抗原特异性。
BEAM 推动科学发展的一些方式
在单次实验中对多达 15 种抗原进行多重分析和筛选将如何推动您的研究?捕获全面的细胞图谱(包括基因表达、全长配对 V(D)J 序列以及抗原特异性)有哪些好处?我们有一些想法。
01
抗体发现
假设您是一名传染病研究人员或开发靶向免疫疗法的临床科学家。您正在寻找已知抗原靶点的有效抗体,比如病毒肽段或癌细胞表面受体。这些抗原靶点带有不同的表位,所以不同的抗体以不同的亲和力与之结合。此外,随着病毒或细胞的进化,它们常常会突变或重组,这也会改变抗体的亲和力。通过一种更全面的抗原组合来筛选 B 细胞可以增加您找到最高效的中和抗体的机会。
在最近的一项内部研究中,10x Genomics 的科学家验证了这种方法,他们使用 BEAM-Ab 来鉴定针对 SARS-CoV-2 刺突蛋白的抗原特异性免疫细胞(点击阅读原文下载研究梗概总结)。他们开发出三种抗原的组合,其中包括融合前的刺突蛋白三聚体(如刺突抗原 S 三聚体和 D614G 三聚体)和一种人类对照蛋白,然后对来自 COVID-19 恢复期患者的 PBMC 进行了分析。在为期一周的分析流程中,他们鉴定出数百种抗原特异性的 B 细胞克隆型。还获得了特定 BCR 的全长配对 V(D)J 序列,可用于快速生产重组抗体以便进行下游验证。除了这项研究,我们期待这个流程能够助力快速可靠的抗体发现。
B 细胞和抗体
02
癌症免疫疗法
我们才刚刚认识到免疫疗法在抗击癌症时有多强大,而 BEAM 有望加速重要的肿瘤学转化研究。假如您有兴趣鉴定患者体内特异性靶向癌症新抗原的 T 细胞——新抗原(neoantigens)是指来源于患者癌细胞的抗原,免疫系统可将其识别为外源蛋白并随后作为靶点。一名患者可能有数十个候选物,可作为理想的新抗原靶点,这凸显了通过 BEAM-T 进行多重抗原筛选的价值,有望揭示患者样本中所有的抗原特异性 T 细胞克隆型。
研究人员可利用 BEAM-T 带来的无以伦比的细胞分辨率来评估 T 细胞表型,更好地了解抗原与受体的相互作用如何影响效应子功能,并最终指导个性化癌症疫苗的开发。获得全长配对的 TCR 序列为研究受体在过继细胞疗法(如 CAR T 细胞疗法)中的潜力开辟了一条道路。
T 细胞在攻击癌细胞
03
疫苗开发
在传染病的军备竞赛中,我们需要使用可获得的所有工具来更好地了解对病原体和疫苗的细胞和分子免疫应答。假设您正试图了解哪种抗原肽会在体内产生最强的抗病毒免疫应答,为疫苗开发提供信息。有了 BEAM-T,您能够在单次实验中筛选多个病毒肽段,包括来自同一种病毒不同毒株的抗原,以便追踪它们对 T 细胞免疫应答的影响。您可以鉴定哪些抗原驱动了独特的免疫应答,最终为多价疫苗的开发提供信息,以确保疫苗对所有病毒株具有最广泛的保护力。
BEAM 技术将大大推动我们对传染病生物学的理解,并加速发现在治疗上具有理想特异性的极其罕见的单克隆抗体。BEAM 流程生成了丰富而强大的数据,有助于我们了解耐受变异的免疫力,并将在耐用疫苗的设计和开发中发挥关键作用。
Bryan Briney 博士
斯克里普斯研究所的助理教授
SARS-CoV-2 病毒被血细胞包围
04
从受体数据库到功能的了解
最近有多个免疫联盟(比如免疫学基因组计划)成立,以建立 BCR/TCR 库数据的大型资源库,反过来,也为共享这些大型数据集建立了标准流程,便于人们更好地利用资源库数据了解免疫介导的疾病和疗法。
BEAM 有着独特的优势,能够以前所未有的方式扩展这些统计工作,帮助人们快速获得以往无法获得的抗原特异性 BCR/TCR 库的数据。以这些数据作为跳板,有望加快疫苗开发,追踪自身免疫性疾病和传染病中的免疫应答,并鉴定新的癌症疗法。
BEAM 如何揭示免疫潜能
BEAM 是一种寻找与治疗相关的抗原特异性 B 细胞和 T 细胞克隆型的变革性方法,简化了往往充满挑战和延误的过程。不过,真正体现其价值的将是科学家们的创新和巧思,他们提出新的想法和应用,以实现他们的登月计划——新的治疗和治愈方法。
BEAM 揭开了免疫复杂性的一层面纱,这种复杂性从单细胞延伸到组织,甚至更远。深入了解抗原特异性克隆型引出了新的问题。哪些免疫细胞能够渗透到肿瘤微环境?您如何在真实组织的背景下追踪和了解与治疗相关的 TCR 的功能?
这些是 10x Genomics 期待与科学家们一起回答的问题,科学家们每天都在激励和挑战我们去突破可能的边界。
如果您对我们的产品和技术感兴趣
欢迎识别下方二维码

内容审核:潘成
项目审核:朱超敏
题图来源:10x Genomics
文章来源:10x Genomics
参考文献:
[1]. Dr. Biology. "B-cells". ASU - Ask A Biologist. 16 February, 2011. https://askabiologist.asu.edu/b-cel
[2]. Dr. Biology. "T-cells". ASU - Ask A Biologist. 16 February, 2011. https://askabiologist.asu.edu/t-cell
[3]. Hoehn K, et al. The diversity and molecular evolution of B-cell receptors during infection. Mol Biol Evol 33: 1147–1157 (2016). doi: 10.1093/molbev/msw015
[14]. Lythe G, et al. How many TCR clonotypes does a body maintain? J Theor Biol 389: 214–24 (2016). doi: 10.1016/j.jtbi.2015.10.016
[5]. https://www.cancer.gov/publications/dictionaries/cancer-drug/def/anti-pd-1-monoclonal-antibody-medi0680
[6]. Mackensen A, et al. Anti-CD19 CAR T cell therapy for refractory systemic lupus erythematosus. Nat Med 28: 2124–2132 (2022). doi: 10.1038/s41591-022-02017-5
[7]. DeMaio A, et al. The role of the adaptive immune system and T cell dysfunction in neurodegenerative diseases. J Neuroinflammation 19: 251 (2022). doi: 10.1186/s12974-022-02605-9
[8]. Mitra S and Tomar PC. Hybridoma technology; advancements, clinical significance, and future aspects. J Genet Eng Biotechnol 19: 159 (2021). doi: 10.1186/s43141-021-00264-6