最近,师妹养的细胞状态越来越差,就算复苏新的细胞种子,状态也依然好不了。一开始也以为是人为操作原因,但仔细讨论分析后才发现,原来是我们养细胞一直忽略的盲区所导致。

师兄,我新买的细胞因子,和你买的 Datasheet 参数差不多,但是内毒素指标不同,细胞状态就相差甚远,难道是它的原因?
要了解问题所在,首先我们得明白内毒素是什么?
内毒素(Endotoxin)是革兰氏阴性菌的细胞壁外壁层上的特有成分,主要由多糖、脂质和蛋白质组成复合体。只有当细菌死亡自溶或用人为破坏后才释放出来表现其毒性。内毒素直接作用于人体时,激活组织内的炎性细胞和炎症因子,导致机体发热并引发全身性炎症反应。
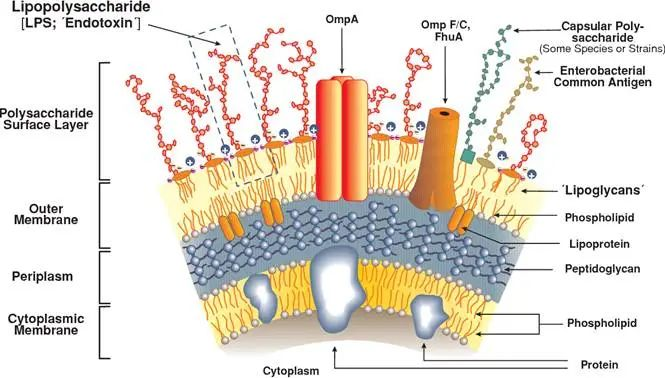
革兰氏阴性菌细胞壁结构,图片来源 DOI:10.1177/09680519010070030101
内毒素会影响重组蛋白的使用吗?
内毒素与细胞膜上的受体结合引起免疫反应,对细胞有较强的毒性作用,从而影响体内或体外细胞的生长和功能。因此,在免疫学实验、细胞培养实验、细胞治疗、细胞凋亡研究以及干细胞培养与扩增分化中,使用的蛋白因子都要求低内毒素。在细胞因子功能分析、蛋白相互作用等研究中也必须使用低内毒素的重组蛋白。以重组蛋白作为抗原,生产高质量的抗体更是需要低内毒素的重组蛋白。

怎么挑选低内毒素的重组蛋白?
优质的重组蛋白在表达纯化过程中,特别注重水质要求,一般会使用注射级别用水,尽量减少内毒素的产生。此外,高通量亲和纯化系统,本身就是一种去除内毒素的理想方法。在蛋白纯化过程中,采用亲和层析过柱法,也能降低产品的内毒素含量。当然如果拥有 GMP 生产线,就能使得整个制备过程无菌,让重组蛋白的内毒素含量低于 0.01 EU/μg。
使用时,业内要求内毒素含量在体外细胞分化培养需 < 1 EU/μg,小鼠药效评价需 < 0.1 EU/μg。当然无论做哪类实验,重组蛋白的内毒素一定是越低越好!

成功挑选低内毒素的重组蛋白后,是否需要区分带有不种类标签的商品化重组蛋白,如果购买了带标签的蛋白,会影响后面的实验吗?
融合标签是指利用 DNA 体外重组技术,在目的蛋白 N 端或 C 端进行融合表达的特定蛋白、多肽或寡肽标签。通过融合标签与包被在固相基质上的特异配基结合,可以使重组蛋白定向固定并得以纯化,大大简化了重组蛋白的纯化。同时,它既保留了天然蛋白的大部分结构,又能实现增加溶解度、防止降解、促进分泌、便于纯化等功能。
重组蛋白的纯化一般分为标签蛋白纯化和无标签蛋白纯化,无标签蛋白纯化比较麻烦,一般需要根据蛋白质本身特定序列来选择多种纯化方法,只通过一种方法很难得到纯度较高的蛋白。虽然麻烦,但是无标签蛋白与天然蛋白有着相同的序列,更有利于蛋白结晶和蛋白功能研究。
较小的融合标签,免疫原性弱,对蛋白质的后续应用和研究不会产生影响。但是有些大标签是需要切除的,例如:Dsb 蛋白、FkpA 蛋白、GST 蛋白、SUMO 标签等。
主要融合标签的优缺点比较
融合标签 | KDA | 优势 | 劣势 |
His-tag | 0.84 | IMAC 填料成本较低,载体的广泛应用, 且有对标签的商业化抗体,标签尺寸小 | 特异性低,纯化纯度较低 |
FLAG | 1.01 | 易剪切,有对应的抗体 | 亲和填料成本高 |
CBP | 2.96 | 温度的洗脱条件 | 一些真核蛋白可能影响其与填料的结合 |
c-myc | 12 | 易于检测 | 纯化成本高 |
ELP | 9~36 | 无需填料纯化 | 需要筛选标签的类型和位点 |
HA | 1.1 | 易于检测 | 纯化成本高 |
GST | 26 | 促进表达,纯化成本较低 | 增溶能力一般 |
Strep II | 1.06 | 特异性较好, 纯化成本相对较低 | 纯化成本比 IMAC 略高 |
MBP | 42 | 促进表达、增溶 | 目的蛋白可能会影响其与填料的结合 |
Trx | 12 | 促进表达、增溶 | 需要额外的亲和标签 |
NusA | 55 | 促进表达、增溶 | 需要额外的亲和标签 |
Bio-Techne 作为第一家商业化生产 TGF-β1 重组蛋白的厂家,对重组蛋白家族的研究工具有多年的研发经验沉淀!如果您想尝试一下优质稳定的重组蛋白产品,把握机会!现Bio-Techne 双十一钜惠开启,买二赠一,限时抢购 ing!


内容审核:邹礼平
项目审核:陆雯芸
题图来源:图虫创意
点击「阅读原文」,了解更多活动详情~
