经常做 western blot 的同学
通常会有一种错觉
这哪里是搞科研
明明是搞「玄学」
十个 WB 七个歪八个丑九个坏
还有一个不出来
要么条带失踪
要么背景漆黑
要么杂带丛生
……
有时就算凑齐天时地利人和
也不一定能得到一组完美条带
江湖传言:一个生物学博士,要跑满 1000 板胶才有可能毕业
WB 实验本身就难
还总是牵涉进
「造假」「撤稿」「学术不端」等丑闻
使得主流期刊对 WB 数据要求越来越高
要求作者提供相关原始数据
甚至要求提供未切割的 WB 全膜条带
对于出道 29 年的大博士而言
WB 的「玄」之操作
它早就积攒了一本厚厚的攻略
【PS:由于排版字数限制,以下分享部分精华】
收获这份攻略
高灵敏度,高信噪比,更低背景……
让你的条带显露真身


跑胶是 WB 实验成败之母
提高跑胶质量的 Tips
蛋白分子量偏高或偏低
可能是胶的浓度与目的蛋白的浓度不对应,比如说 100KD 的蛋白你用 12% 的胶跑,或者说 20KD 的蛋白你用 8% 的胶跑。
蛋白质降解
蛋白质降解后很可能会在比原来位置低的地方出现主带,然后出现一些其他带,最主要的特点是所有的条带比正常的都低,并且条带模糊不清晰。
所有条带连成一片无间隔
最可能是上样量过多,其次是样品弥散(比如电泳长时间停止样品弥散)。
溴酚蓝拖尾
样品溶解不好或上样前未变性完全。
纵向的纹理
上样样品中存在不溶性颗粒。
溴酚蓝很粗
浓缩胶浓缩效果不好,可能是浓缩胶太短或者配错。
在分离胶中跑不动
Tris-Cl pH 值不对,或者忘记加 SDS。
BOSTER
#1/无背景无条带
www.boster.com.cn

原因分析
如果 marker 正常,其他位置没有条带,最可能是一抗加成其他抗体,或者二抗种属加错了,比如兔的加成鼠的。
解决办法
a. 目的蛋白完全无信号,但同时做的内参是正常的,那么大部分情况是一抗抗体失效或用错二抗。
b. 目的蛋白和内参均无信号,则考虑是否发光液失效。如果膜上没有 marker 则为转膜失败。
c. 如果中间出现了细微条带,可能是蛋白上样量太少,或一抗浓度过低。
经验之谈
上图展示一点信号都没有,大部分情况是因为抗体加错了。如果中间出现细微的条带,可能是蛋白上样量太少,一抗浓度过低,ECL 发光液失效。

BOSTER
#2/高背景
www.boster.com.cn
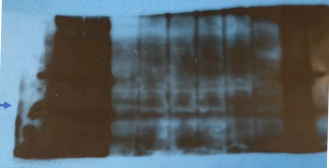
原因分析
封闭不充分,一抗浓度过高,洗膜时间次数不够。
解决办法
降低一抗浓度,增加洗膜时间和次数。
a.一抗/二抗浓度配比不合适:杂带多,大概率是抗体特异性不好,也有可能抗体浓度太高,可尝试降低一抗浓度进行实验。
b.封闭液问题:配制封闭液所用的脱脂奶粉应选用无防腐剂实验专用脱脂奶粉。
c.洗膜不充分:洗膜按规定来 5min*5 次或 10min*3 次。
经验之谈
高背景是 WB 实验中最常见的问题,目的条带单一清晰,但其他地方又弥漫性较均一的背景(比较连续的)。杂带多大概率是抗体特异性不好,也有可能抗体浓度太高,可尝试降低一抗浓度进行实验。

BOSTER
#3/非特异性条带
www.boster.com.cn
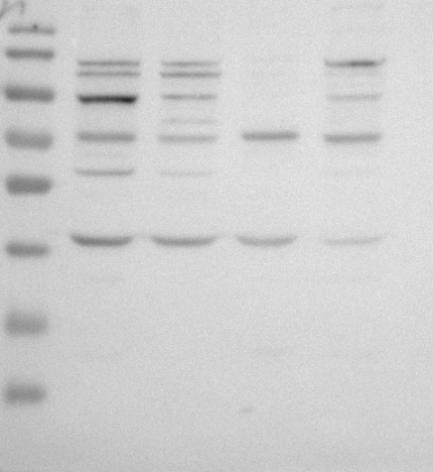
原因分析
一抗非特异性与蛋白结合。
解决办法
更换一抗。
经验之谈
此种情况绝大多数是因为一抗不好,你无法判断哪一条是目的条带。如果实在没有更好的抗体,建议采用阴性对照和阳性对照来确定上述哪个条带是目的条带。当然也有一种很小几率的可能是一抗浓度太高引起的非特异性结合。

BOSTER
#4/条带中出现边缘规则的白圈
www.boster.com.cn
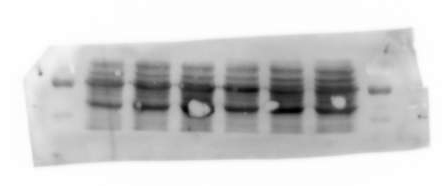
原因分析
a.电转中膜与胶之间存在气泡。
b.可能是转膜过程烧膜了,特别是半干转操作不当导致烧膜。
c.转膜时温度过高产生气泡。
d.印迹膜活化不佳。
解决办法
a.注意排清气泡。
b.优化实验条件或使用湿转法转膜。
c.把整个转膜装置放于 -20 度冰箱中电转。
d.确保印迹膜完全活化。
经验之谈
我们常常将电转液倒入一个盘子里,倒入的液体不宜太多或太少,建议高度与放上第一层滤纸齐平,然后往滤纸上浇点转膜液,往胶上面浇点电转液,用两只手的拇指和食指轻轻夹住 NC 膜的两侧中间,使膜成 U 型,然后将 U 型底部接触胶的中间,慢慢往两边放下膜,这样一般气泡很少。然后上层滤纸同样用 U 型的放置方法,用玻璃棒稍微贴实下,最后盖上海绵。

BOSTER
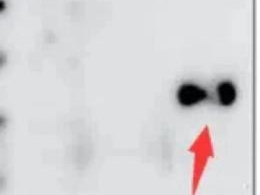
#5/出现黑点和黑斑
www.boster.com.cn
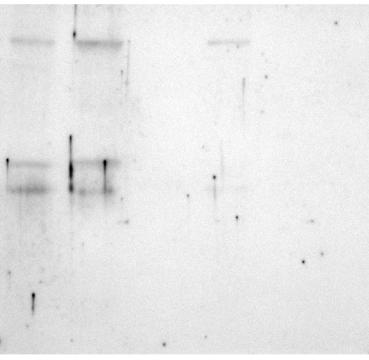
原因分析
a.一般出现这种情况可能是封闭液溶解不完全或封闭液存放时间太久(长菌)。
b.膜上其他部位与一抗或二抗非特异性结合。
解决办法
a.过滤封闭液或选用其他类型封闭液。
b.与其他品牌已验证过好用的抗体处理相同样本,作比较,看是否还有斑点。
经验之谈
牛奶溶解后,最好静止一下,然后轻轻吸取上层牛奶进行封闭,封闭结束后一定要洗 3 遍之后再加一抗。

BOSTER
#6/条带拖尾
www.boster.com.cn
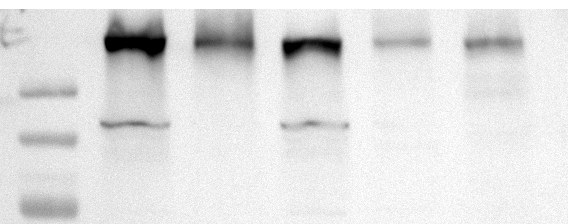
原因分析
一抗浓度太高和时间太长。
解决办法
根据情况调整一抗浓度,时间也可缩短。
经验之谈
这种情况一般出现在大分子量抗体实验中,是因为一抗浓度太高,作用时间太长引起的。另外洗一抗和洗二抗千万不要偷工减漏,建议 5min*5 次,不要担心洗这么多次把抗体和蛋白洗掉了,真正的抗原抗体相结合通过这种方式是洗不掉的。

BOSTER
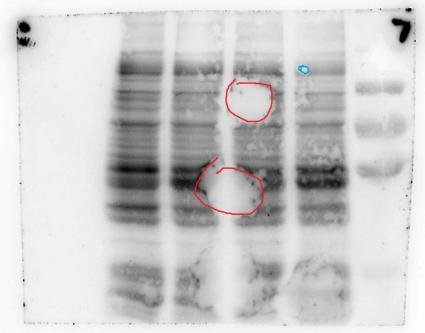
#7/出现非均一性背景
www.boster.com.cn
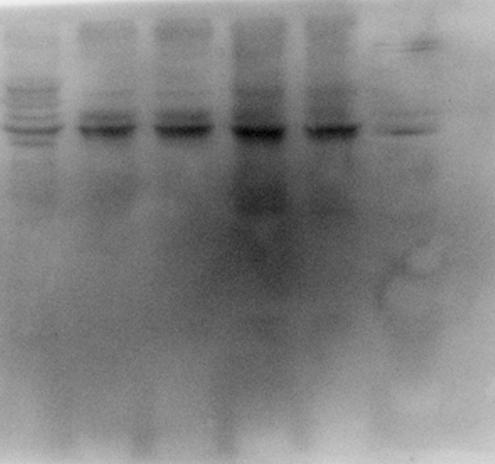
原因分析
膜可能在孵育或洗涤过程中干过。
解决办法
每一步的操作过程中,注意不要让膜干。
经验之谈
封闭时洗一抗洗二抗,以及发光时都应时刻注意切记蛋白面风干,一旦风干很可能会导致这个结果。

BOSTER
#8/某个条带变形
www.boster.com.cn
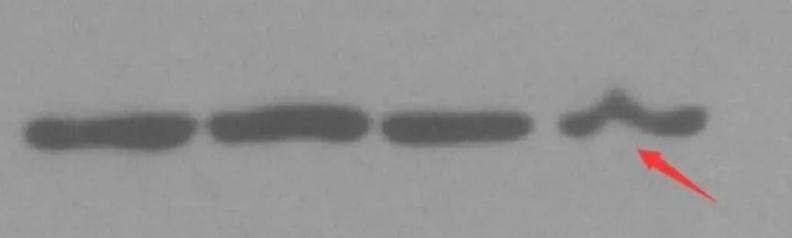
原因分析
SDS-PAGE 胶中存在气泡或某不溶性颗粒。
解决办法
配胶过程中,要注意不要使用无杂质液体。
经验之谈
很多实验室中使用的不是最新设备,比如配胶用的海绵垫,如果用了很多年,会从下面往上面漏小气泡,当气泡足够小并且胶快凝固的时候,走到中间的小气泡就停留在胶内,并会影响到后面的跑胶。另外配胶用的水,SDS,Tris 缓冲液要注意不要有杂质。

BOSTER
#9/条带不均一
www.boster.com.cn
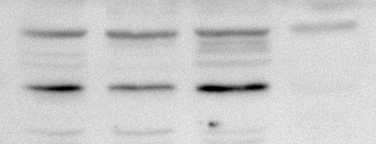
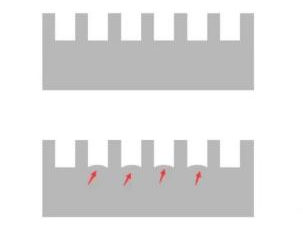
原因分析
a.配置胶凝固不均一。
b.转膜问题:转膜夹子不紧,转膜滤纸或海绵由于使用消耗,滤纸及海绵变薄,海绵弹性不足。
c.一抗孵育问题:抗体孵育不充分或抗体稀释液放入过少。
解决办法
a.把胶配好,不合格的胶坚决不用。
b.及时更换转膜滤纸和海绵。
c.增大抗体稀释液用量、更换跷跷板类型的摇床将膜完全进入抗体稀释液中。
经验之谈
出现哑铃最大的可能是胶没有配好,胶凝固后不均一。如果你拔完梳子后出现上图中下面部分的情况,多半会出现哑铃状。另外还有一种可能是样品中含有太多杂质,没有离心下来,然后杂质沉积在孔的中间,蛋白自然被推挤到两边。

BOSTER
#10/最边缘条带弯曲
www.boster.com.cn
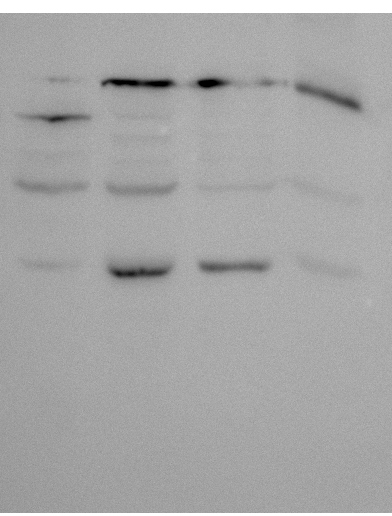
原因分析
电泳电流不均一,玻璃板右下侧有缺口。
解决办法
换用新的玻璃板,不使用两边的两孔。
经验之谈
一般我们使用的是 10 孔的胶,如果你上样刚好 10 个孔,那么最两头的两个孔肯定会歪曲。另外上样最好在胶的中间,这样电场均一。

BOSTER
#11/条带笑脸,marker正常
www.boster.com.cn
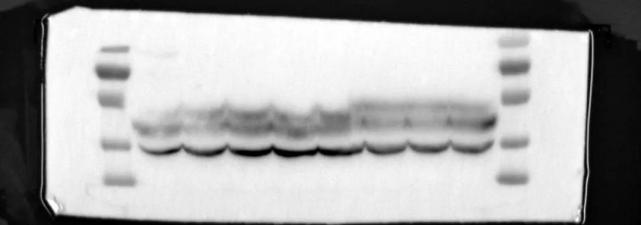
一般来说笑脸问题首先考虑电泳环节,多半是凝胶没凝固好。但上图 marker 却异常整齐,笑脸条带整齐地手拉手,这就不是凝胶问题导致的。
原因分析
a.loading buffer 失效,导致样品变性失败。
b.上样量过大或样品杂质多。
c.电压太高。
解决办法
a.更换 loading buffer。
b.超滤样品或降低上样量。
c.降低电压。
经验之谈
准备样本主要确认上样缓冲液是否为近期配置,并且要妥善保存,否则就会浪费珍贵的实验样本。一般电泳过程中恒压电泳,浓缩胶 80V,分离胶 120V,整个过程差不多需 2 个小时左右。

BOSTER
#12/曝光结果条带扭曲
www.boster.com.cn
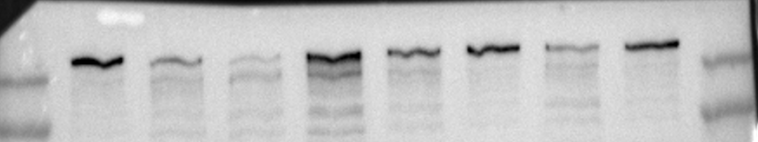
原因分析
转膜问题,对于分子量稍大的蛋白,转膜时间过长,转膜装置产热过多,无法维持转膜时的低温环境,造成条带扭曲。
解决办法
建议在条件允许的情况下直接在 4℃ 中进行转膜,将冰更换为冰水混合物,及时更换转膜液并将转膜液放入 4℃ 中提前预冷。
经验之谈
对于大分子量的抗体,跑胶前可以先把样本煮一下,然后稍微离心一下,同样也可以改善这种情况。

BOSTER
WB实验操作视频
www.boster.com.cn
高清完整版!
完整的 WB 实验包括了很多步骤,从蛋白提取到配胶、上样电泳,再到转膜、封闭,最后孵育一抗二抗后才能去进行检测。时间跨度非常长,而且这中间的每一步都包含了很多小细节,稍有不慎就会导致结果出错,然后又得从头来过。
以下是大博士出品的 WB 实验操作视频,手把手教大家如何对实验步骤关键点进行精细化操作。
【点击放大观看】

BOSTER
实验技术手册
www.boster.com.cn
干货福利免费领!
本实验技术手册为博士德资深技术人员根据多年实战经验呕心沥血编写,围绕以下目录中八大核心技术内容展开,无论对于科研萌新或实验达人都是满满的纯干货。


BOSTER

【扫码下载收藏】
想跑出漂亮的条带图
除了实验精细化操作
选择靠谱的实验试剂
同!样!重!要!
BOSTER
买一抗送二抗
买 ELISA 送好礼


内容审核:康晋伟
项目审核:朱超敏
题图来源:博士德