(周五晚实验室组会上,轮到我汇报本周进展。由于一周数据失败,前后两次实验的结果不一致,所以没有准备汇报 PPT)

导师

你这周啥也没干?为什么没准备 PPT ?
?
这周数据都不太好,没什么可呈现的
 。
。


我

导师

失败的数据才更需要拿出来分析,你有分析原因吗?
我按照 MIQE 指南里 qPCR 的实验步骤一步步操作的,设计了 PCR 引物,也进行了退火温度的摸索,但结果就是不一致。


我

师姐

应该不至于, MIQE 指南里相关要求写得很详细,里面有一个很重要的环节就是对你 qPCR 检测方法的分析性能进行验证,你做过验证吗?
没有,做了会怎么样啊
 ?
?


我

师姐

性能验证能帮助你获得稳定、可靠和准确的实验数据。没事儿,我教你。
好,下周组会我一定好好准备

 !
!


我

导师

回头记得把 MIQE 指南发到群里,实验室每位同学都应该好好学习一下。

识别对话框中二维码即可下载完整版《实时荧光定量 PCR 国际化标准-MIQE 指南》。


我
一、为什么要做 qPCR 检测方法的验证
任何实验的目的都是为了获得稳定、可靠和准确的数据,检测方法的验证在其中起着极为重要的作用。验证的结果可以用于判断分析结果的质量、可靠性和一致性,这是所有实验质量控制体系不可分割的一部分,MIQE 也要求对 qPCR 检测方法的分析性能进行验证,具体如下:
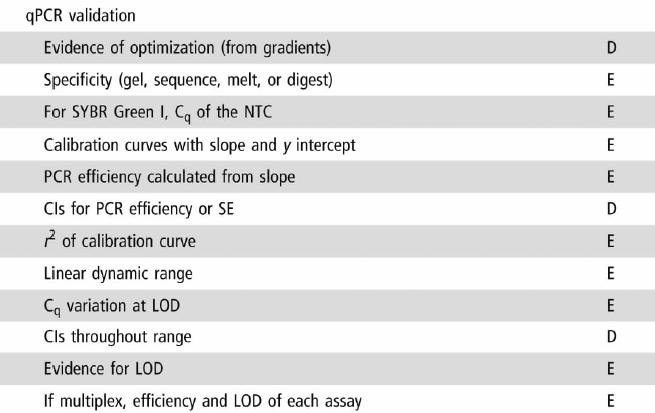
图片来源. MIQE指南,doi: 10.1373/clinchem.2008.112797. Epub 2009 Feb 26.
二、常见的误区

 误区:仅通过 Cq 值和标准偏差值 SD 来判断数据结果是否一致或者仅通过单个引物或单个数据点的 Cq 值来评估检测性能的好坏。这种做法比较常见,但显然不恰当,因为:
误区:仅通过 Cq 值和标准偏差值 SD 来判断数据结果是否一致或者仅通过单个引物或单个数据点的 Cq 值来评估检测性能的好坏。这种做法比较常见,但显然不恰当,因为:
● 阈值线 threshold 的设置能直接改变 Cq 值的大小,且 C 值要在有参照系的情况下才有意义,比如绝对定量时,或者相对定量时的 △Cq 或者 △△Cq ;
● 不同试剂的组分不同(如阳离子,PH 值,染料种类或浓度)也会影响 Cq 值的大小;
● PCR 扩增效率比 Cq 值本身更重要,例如同样的样品,一次实验的 Cq 值是 21,扩增效率是 80%,另一次实验 Cq 值是 22,扩增效率是 95%,重复性特异性都好,显然 Cq 值为 22 的结果更可靠。
三、 qPCR 检测方法的分析验证有哪些内容?
Bio-Rad 作为国际领先的 qPCR 仪器和试剂耗材的生产商,积极倡导 MIQE 指南并根据其中的观点设计分析验证实验,帮助大家评估商业化试剂效果。
验证检测方法的可靠性及评估所选试剂的效果可通过模板梯度稀释实验来评估,可得到除了 Cq 值外的更多信息,包括:
● 效率
效率不仅是 PCR 效率,还包含反转录(Reverse transcription,RT)的效率。RT 效率是指 RNA 合成 cDNA 的效率,如果 1,000 个 RNA 分子变成 1,000 个 cDNA 分子,效率就是 100% ,实际上很多 RT 酶的效率对于不同浓度的 RNA 样本存在差异,这样 cDNA 扩增后的结果并不能真实反映样品中 RNA 的水平。PCR 效率是指 DNA 在扩增的每个循环中复制的效率,每个循环增加 2 倍,其效率就是 100% ,这也和所选试剂、引物、模板质量密切相关;
● 线性
梯度稀释实验得到的标准曲线可直观地显示各浓度理论值和测得的 Cq 值的相关性,其中 R2 值表示各个数据点是否正好落在标准曲线上,当 R2 < 0.98 时,表明数据偏差较大;
● 动态范围
指在可靠( R2 > 0.98,效率 90~110% 即斜率 - 3.6 至 - 3.1)的数据范围内,样品的检测范围( RNA 或 DNA 的最高检测限和最低检测限),可靠的 Cq 值一定要在这个范围内;
● 灵敏度
灵敏度是指梯度稀释后,能可靠检测到( R2 > 0.98, 效率 90~110%)的最低样品浓度。除了试剂因素,灵敏度与引物设计、样品的类型和模板质量都有关系;
● 特异性
染料法如 SYBR Green 可以通过熔解曲线直接来判断,如果是探针法可以通过凝胶电泳或测序来验证;
● 重复性
重复性包含生物学重复(样品不同)及技术重复(复孔)。生物学重复性受样品本身的个体差异及样品收集和核酸纯化的方式影响较大,技术性重复受试剂、反应管、移液操作及仪器本身影响较大,复孔差异的 SD 在 0.5 以内,说明数据比较可靠。
四、如何开展 qPCR 检测方法的分析验证
在检测大量样品前,每对引物都需要用对照样品进行梯度稀释实验,以验证方法和数据的可靠性。如果是评估商业化试剂,则最好使用内参基因和高、中、低丰度的目标基因来做梯度稀释实验,这样可以更全面地了解检测方法的分析性能。
分析性能验证 & 试剂评估实验设计:
(一)RNA 梯度稀释实验 — 验证反转录效率的一致性
同一个基因 RNA 在不同样品间表达水平可能有高有低,无论表达量高低,反转录效率一致的 qPCR 结果才能真正反映 RNA 水平:
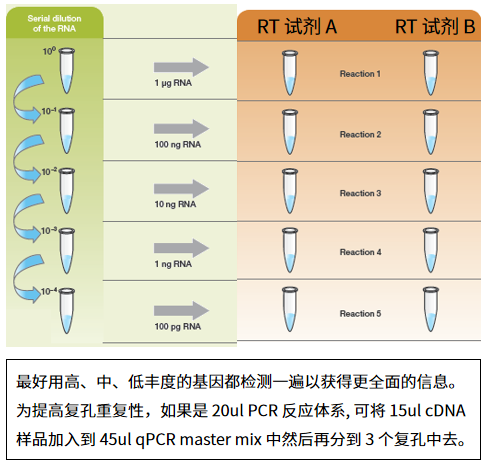
图片来源:伯乐生命科学
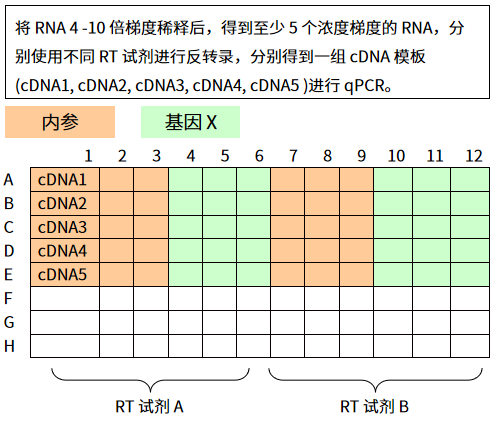
图片来源:伯乐生命科学
(二)cDNA 或者 DNA 梯度稀释实验 — 验证 PCR 步骤的可靠性
将 cDNA 或者 DNA 进行 4~10 倍梯度稀释,得到至少 5 个浓度梯度的 cDNA(cDNA1,cDNA2,cDNA3,cDNA4,cDNA5),分别使用 qPCR supermix A,qPCR supermix B 针对同样的模板进行检测。

图片来源:伯乐生命科学

图片来源:伯乐生命科学
以上就是这次为大家介绍的 qPCR 检测方法的分析性能验证方法,希望能对大家的日常科研工作有所帮助~
Bio-Rad 为您提供完整的基因表达分析解决方案,全面满足您的需求~
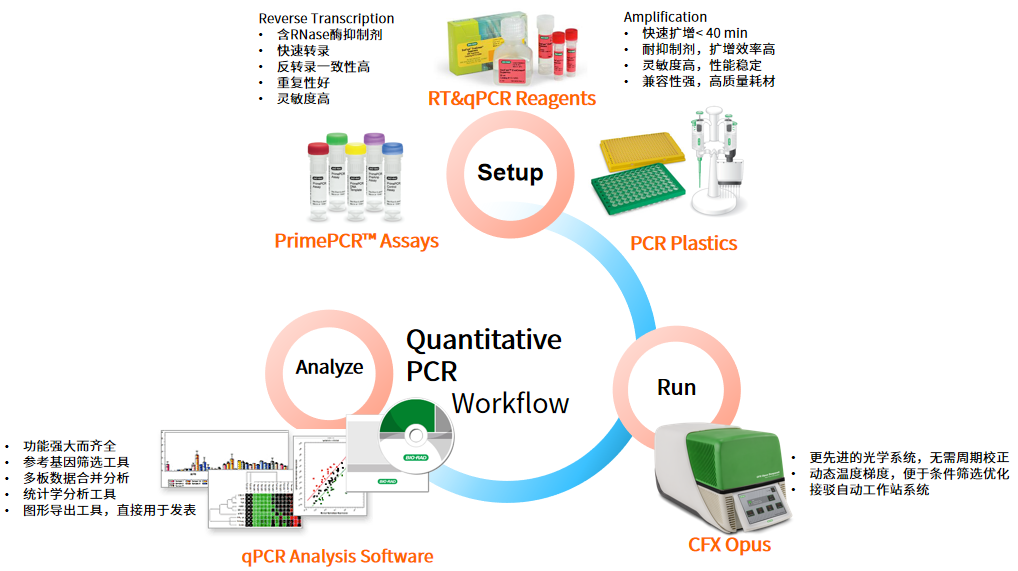
图片来源:伯乐生命科学
Bio-Rad,您身边的 qPCR 专家!
* BIO-RAD 是 BIO-RAD LABORATORIES, INC. 在特定区域的商标。
* 本产品仅用于科研用途,不用于临床诊断。
相关阅读:IF 17+ 的文章被撤稿,没想到大咖也会犯这种错误
内容策划:王丹琦
内容审核:周育红
题图来源:站酷海洛
参考资料:
[1]. Bustin SA, Benes V, Garson JA, Hellemans J, Huggett J, Kubista M, Mueller R, Nolan T, Pfaffl MW, Shipley GL, Vandesompele J, Wittwer CT. The MIQE guidelines: minimum information for publication of quantitative real-time PCR experiments. Clin Chem. 2009 Apr;55(4):611-22. doi: 10.1373/clinchem.2008.112797. Epub 2009 Feb 26.
[2]. Bio-Rad tech note 5859.
▼ 点击「阅读原文」,即可下载 MIQE 指南~